题目内容
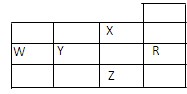
下表为元素周期表前四周期的一部分,下列关于R、W、X、Y、Z五种元素的叙述中正确的是

| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.最高价含氧酸的酸性,Y对应的酸性强于W |
| D.P能级未成对电子最多的是Z元素 |
C
根据元素在周期表中的位置可判断,R、W、X、Y、Z五种元素分别是Ar、P、F、S、
Br。非金属性越强第一电离能越大,但由于P原子中3p轨道电子是半充满状态,所以第一电离
能大于S的,A不正确。B不正确,硫离子和溴离子的核外电子数分别是18和36。非金属性越
强,最高价氧化物的水化物的酸性越强,C正确。P能级未成对电子最多的是P元素,D不正确。
答案选C。
Br。非金属性越强第一电离能越大,但由于P原子中3p轨道电子是半充满状态,所以第一电离
能大于S的,A不正确。B不正确,硫离子和溴离子的核外电子数分别是18和36。非金属性越
强,最高价氧化物的水化物的酸性越强,C正确。P能级未成对电子最多的是P元素,D不正确。
答案选C。

练习册系列答案
相关题目
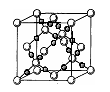
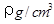 ,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为
,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为 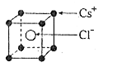
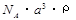 g/mol B.
g/mol B.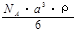 g/mol
g/mol 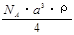 g/mol D.
g/mol D.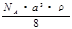 g/mol
g/mol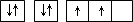
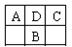 A、C两种元素的原子核外电子数之和等于B原子的核电荷数。有关说法错误的是
A、C两种元素的原子核外电子数之和等于B原子的核电荷数。有关说法错误的是 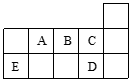 A.C、D气态氢化物稳定性强弱和沸点高低均为C>D
A.C、D气态氢化物稳定性强弱和沸点高低均为C>D