题目内容
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”=SiC______Si;SiCl4______SiO2。
(2)图中立方体中心的“![]() ”表示硅晶体中的一个原子,请在立方体的顶点用“
”表示硅晶体中的一个原子,请在立方体的顶点用“![]() ”表示出与之紧邻的硅原子。
”表示出与之紧邻的硅原子。

(3)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热ΔH=______kJ·mol-1。
Si(s)+4HCl(g),该反应的反应热ΔH=______kJ·mol-1。
解析:本题考查键能的大小与物质性质及反应热之间的关系。
(1)SiC与Si皆为原子晶体,由于Si—C键能大于Si—Si键能,故SiC的熔点比Si高;SiCl4为分子晶体,SiO2为原子晶体,前者的熔点低于后者。
(2)根据硅原子与硅原子可形成四个相等的硅硅键可知,除立方体中心的硅原子外,与它相邻的硅原子应处于可形成正四面体的四个顶点上。
(3)根据题意:所给反应的旧化学键键能之和为:4×360 kJ·mol-1+2×436 kJ·mol-1=2312 kJ·mol-1,新化学键键能之和为4×431 kJ·mol-1+2×176 kJ·mol-1(每摩硅原子相当于形成2 mol Si—Si)=2076 kJ·mol-1,所以反应热为:2312 kJ·mol-1-2076 kJ·mol-1=236 kJ·mol-1。
答案:(1)> < (2)如图
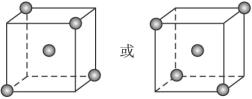
(3)+236

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A、一定温度下,反应Mg(1)+Cl2(g)=MgCl2(1)的△H<0,△S<0 | ||||||||||||
| B、101 kPa时,硫的标准燃烧热与硫完全燃烧时物质的量有关 | ||||||||||||
C、通常人们把拆开1 mol气态物质中某种共价键需要吸收的能量看成该共价键的键能
| ||||||||||||
| D、已知:N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-1 2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1 C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1 则4CO(g)+2NO2(g)=4NO2(g)+N2(g)△H=+1200kJ?mol-1 |
化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
键能kJ·mol | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列物质的熔点高低(填“>”或“<”)SiC__________Si。
(2)下图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。

(3)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)该反应的反应热ΔH=____________kJ/mol。
Si(s)+4HCl(g)该反应的反应热ΔH=____________kJ/mol。
化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
①比较下列两组物质的熔点高低(填“>”或“<”)SiCl4______SiO2;
②工业上用高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热ΔH=_______________kJ/mol。
(2)对于CO中毒、心肌梗塞、冠心病或小儿肺炎等危重患者都要采用吸氧治疗。普通医务室中没有氧气瓶,但一般都有消毒用的30%的H2O2溶液。同时还有可选用的试剂为:KMnO4、H2SO4、K2SO4、Mg、CuSO4、NaCl和葡萄糖。请利用上述试剂写出一种使H2O2中的氧完全释放出来的理想反应的离子方程式: _____________________________________________。
(3)将一定量的硫粉和铁粉的混合物隔绝空气加热,充分反应后冷却,再加入足量的稀硫酸,得到标准状况下的气体
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。现给出化学键的键能(见下表):
|
化学键 |
H—H |
Cl—Cl |
Cl—H |
|
键能/(kJ·mol-1) |
436 |
243 |
431 |
请计算H2(g)+Cl2(g)===2HCl(g)的反应热( )
A.+862 kJ·mol-1 B.+679 kJ·mol-1
C.-183 kJ·mol-1 D.+183 kJ·mol-1
(8分)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si—O |
Si—Cl |
H—H |
H—Cl |
Si—Si |
Si—C |
|
键能/kJ·mol—1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”
SiC Si; SiCl4 SiO2
(2)右图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。

(3)工业上高纯硅可通过下列反应制取:
SiCl4(g) + 2H2(g) 高温 Si(s) + 4 HCl(g) 该反应的反应热△H = kJ/mol.