题目内容
下列叙述中不正确的是
| A.通过化合反应与置换反应均可以制得Fe3O4 |
| B.通过化合反应与复分解反应均可以制得Fe(OH)3、NaHCO3 |
| C.离子化合物的熔点不一定比共价化合物的熔点高 |
| D.向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总物质的量为3 mol |
D
正确,化合3Fe+2O2
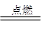 Fe3O4置换 3Fe+4H2O
Fe3O4置换 3Fe+4H2O Fe3O4+4H2↑
Fe3O4+4H2↑正确,化合4Fe(OH)2+O2+2H2O="4Fe" (OH)3 ,Na2CO3+H2O+CO2=2NaHCO3 复分解FeCl3+3NaOH=Fe(OH)3↓+3NaCl,Ba (HCO3)2+Na2SO4=BaSO4↓+2NaHCO3
正确,有些耐高温材料,熔点很高;
不正确,1mol KAl(SO4)2的溶液中加入1.5molBa(OH)2溶液时沉淀质量最大,2.5mol,不可能达到3mol.

练习册系列答案
相关题目
 5g,含有0.6mol Cl-,则该金属为
5g,含有0.6mol Cl-,则该金属为  液能导电
液能导电