题目内容
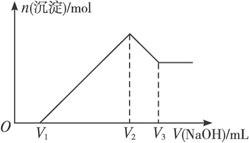
将m g Al2O3和Fe2O3的混合物溶于100 mL盐酸中,然后逐滴加入1 mol·L-1的氢氧化钠溶液,其结果如图1-3-17所示: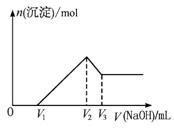
图1-3-17
若保持混合物总质量不变,Al2O3与Fe2O3按不同比例混合进行上述实验(其他条件不变),当![]() 变大时,关于V1、V2、V3的变化的判断正确的是( )
变大时,关于V1、V2、V3的变化的判断正确的是( )
A.V1变大 B.V2不变 C.V3变小 D.(V3-V1)不变
解析:由M(Fe2O3)>M(Al2O3),故等质量的Al2O3和Fe2O3,n(Al2O3)>n(Fe2O3)。由于Fe2O3+6 H+====2Fe3++3H2O;Al2O3+6H+====2Al3++3H2O,所以当![]() 变大时等质量的混合物,消耗酸的物质的量增多,由于盐酸的量是一定的,所以V1减少。又由Fe3++3 OH-====Fe(OH)3和Al3++3 OH-====Al(OH)3知,Al2O3—6 H+—6 OH-—2Al(OH)3,Fe2O3—6H+—6OH-—2Fe(OH)3,所以V2不随
变大时等质量的混合物,消耗酸的物质的量增多,由于盐酸的量是一定的,所以V1减少。又由Fe3++3 OH-====Fe(OH)3和Al3++3 OH-====Al(OH)3知,Al2O3—6 H+—6 OH-—2Al(OH)3,Fe2O3—6H+—6OH-—2Fe(OH)3,所以V2不随![]() 的比值变化而变化,显然V3增大;由于Al2O3溶于盐酸消耗H+的物质的量不等于等量铝的氢氧化物溶于碱消耗OH-的物质的量,故D不正确。
的比值变化而变化,显然V3增大;由于Al2O3溶于盐酸消耗H+的物质的量不等于等量铝的氢氧化物溶于碱消耗OH-的物质的量,故D不正确。
答案:B

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目