题目内容
【题目】碳酸钠、碳酸氢钠是日常生产生活中常用的两种盐。在实验室中制取NaHCO3的方法有多种。请
依据下列方法回答问题:
方法一:模拟工业“侯氏制碱法”制取:(原理NaCl+H2O+CO2+NH3 = NaHCO3↓+NH4Cl)
第一步:连接好装置,检验气密性,在仪器内装人药品。
第二步:让某一装置先发生反应,直到产生的气体不能再在Ⅲ中溶解,再通入另一装置中产生的气体,片刻后,Ⅲ中出现固体。继续向Ⅲ中通入两种气体,直到不再有固体产生。
第三步:分离Ⅲ中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的某固体粉末,有NH4Cl晶体析出。
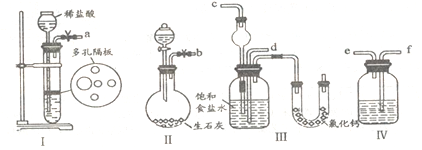
(1)图中所示装置的连接顺序是:a接f;e接________;b接_________(填接口编号)。
(2)I中盛放稀盐酸的仪器名称是_____________,IV中应选用的液体为________________。
(3)第二步中让_____________ (填序号)装置先发生反应。
(4)第四步中所加固体粉末为________。所得的晶体中常含有少置的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所得晶体大部分是NH4Cl。简要写出操作和现象______________________。
方法二:把CO2通人饱和Na2CO3溶液制取NaHCO3。装置如下图所示(气密性已检验,部分夹持装置略):

(5)请结合化学平衡移动原理解释B中溶液的作用_________________。
(6)当C中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设计方案如下(取一定量的固体,配成溶液作为样液,其余固体备用):
①方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是________________。
②方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是________________。
【答案】 d c II 饱和碳酸氢钠溶液 NaCl 取少量固体放入试管中,加热,固体大部分消失,在试管口内壁又有较多的固体凝结。 CO2在水中存在平衡:CO2+H2O![]() H2CO3
H2CO3![]() HCO
HCO![]() +H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体。 Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3。 2HCO
+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体。 Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3。 2HCO![]() +Ba2+ = BaCO3↓+ CO2↑+H2O NaOH + CO2=NaHCO3; Ca(HCO3)2+ NaOH== NaHCO3+ CaCO3 +H2O
+Ba2+ = BaCO3↓+ CO2↑+H2O NaOH + CO2=NaHCO3; Ca(HCO3)2+ NaOH== NaHCO3+ CaCO3 +H2O
其它合理方法均可。
【解析】本题考查实验设计方案的评价,(1)装置I是制备CO2,装置II制备氨气,因为氨气极易溶于水,为防止倒吸,因此b接c,制出的CO2中混有HCl,必须除去,因此a接f,e接d;(2)盛放稀盐酸的装置是长颈漏斗,除去CO2中的HCl,常通过饱和碳酸氢钠溶液,即装置IV中盛放饱和NaHCO3溶液;(3)因为CO2在水中的溶解度小,氨气极易溶于水,且水溶液显碱性,为充分利用CO2,减少浪费,因此先通NH3,让装置II先反应;(4)第四步中加固体NaCl,让NH4Cl晶体析出;具体操作是:取少量固体放入试管中,加热,固体大部分消失,在试管口内壁又有较多的固体凝结;(5)CO2在水中存在平衡:CO2+H2O![]() H2CO3
H2CO3![]() HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体;(6)①Ca(OH)2与Na2CO3反应:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,碳酸氢钠与Ca(OH)2反应:Ca(OH)2+NaHCO3=CaCO3↓+H2O+NaOH,两个都会产生沉淀,因此Na2CO3对NaHCO3检验产生干扰;②沉淀是BaCO3,气体是CO2,因此有2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O。
HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体;(6)①Ca(OH)2与Na2CO3反应:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,碳酸氢钠与Ca(OH)2反应:Ca(OH)2+NaHCO3=CaCO3↓+H2O+NaOH,两个都会产生沉淀,因此Na2CO3对NaHCO3检验产生干扰;②沉淀是BaCO3,气体是CO2,因此有2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案