题目内容
【题目】下列说法正确的是
A.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色
B.二氧化氯和三氯化铁都常用于自来水的处理,二者的作用原理相同
C.Ksp不仅与难溶电解质的性质和温度有关,而且还与溶液中的离子浓度有关
D.7.8g过氧化钠含有的共用电子对数为0.1NA
【答案】D
【解析】
A、聚乙烯中不含碳碳双键,不能和溴水发生加成反应而使溴水褪色,错误;
B、二氧化氯用于自来水的处理是利用其强氧化性来杀菌、消毒,三氯化铁用于自来水的处理是利用其水解生成的氢氧化铁胶体吸附水中悬浮的杂质而沉淀下来,二者的作用原理不同,错误;
C、Ksp只与难溶电解质的性质和温度有关,而且与溶液中的离子浓度无关,错误;
D、过氧化钠的电子式为![]() ,7.8g过氧化钠的物质的量为0.1mol,含有的共用电子对数为0.1NA,正确;
,7.8g过氧化钠的物质的量为0.1mol,含有的共用电子对数为0.1NA,正确;
答案选D。

【题目】某学生用0.1500moVL标准盐酸测定某未知浓度的NaOH溶液,其操作可分解为如下几步:
A.用蒸馏水洗净滴定管
B.用待测定的溶液润洗碱式滴定管
C.用碱式滴定管取NaOH溶液25.00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作2~3次
E.检查滴定管是否湍水
F.取下酸式滴定管用标准盐酸润洗后,将标准液注入酸式滴定管“0"刻度以上2~3cm处,再把酸式滴定管固定好,调节液面至0"刻度或“0"刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)滴定时正确操作的顺序是(用字母填写)____________________
(2)本实验中对滴定管的操作如下图所示,正确的是______________(填字母)。
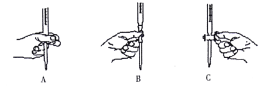
(3)判断到达滴定终点的现象是________________________________________
滴定结果如下表所示:
滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 0.60 | 20.60 |
3 | 25.00 | 0.20 | 20.19 |
计算该NaOH溶液的物质的量浓度为_____________mol/L
(4)下列操作会导致测定结果偏高的是________
A.酸式滴定管在装液前未用标准盐酸润洗
B.滴定过程中,锥形瓶摇晃的太剧烈,锥形瓶内有液体溅出
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
【题目】下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 取1mL20%蔗糖溶液,加入适量稀硫酸,水浴加热后取少量溶液,加入几滴新制的Cu(OH)2悬浊液,加热没有砖红色沉淀生成 | 溶液中未出现砖红沉淀 | 蔗糖未水解 |
B | 将C和SiO2的固体混合物加热加热 | 2C+SiO2 | 非金属性:C>Si |
C | 向盛有2mL0.1molL-1的NaCl溶液的试管中逐滴加入几滴0.1molL-1AgNO3溶液,充分反应后,再逐滴加入AgNO3溶液,充分反应后,再逐滴加入0.1molL-1的KI溶液 | 白色沉淀变为黄色沉淀 | Ksp(AgCl)>Ksp(Agl), |
D | 向待测液中加入适量的稀NaOH溶液,将湿润的蓝色石蕊试纸放在试管口 | 湿润的蓝色石蕊试纸未变红 | 待测液中不存在NH4+ |
A.AB.BC.CD.D
【题目】下表是三种银盐的溶度积常数Ksp(25℃ ).下列说法不正确的是
化学式 | AgCl | AgBr | AgI |
颜色 | 白 | 浅黄 | 黄 |
Ksp(25℃) |
|
|
|
A.25℃ 时,三种银盐的饱和溶液中,c(Ag+)最大的是AgCl溶液
B.在AgCl的悬浊液中加入0.1mol·L—1的KI溶液,可能有黄色沉淀产生
C.25℃ 时,AgC1固体在等物质的量浓度的NaC1,CaC12溶液中的溶度积相同
D.在AgBr的悬浊液中加入0.1mol·L-1的KI溶液,发生反应的离子方程式为 ![]()