题目内容
【题目】实验室中要测定部分变质的过氧化钠的纯度,可用如图装置实现。
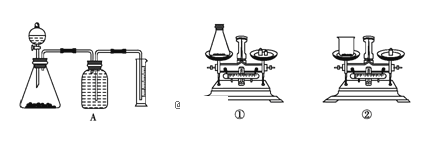
(1)锥形瓶中应放______,分液漏斗中放______,锥形瓶中发生反应的化学方程式为_______________________________。
(2)如图用托盘天平称取样品,应选用如图中的____(填“①”或“②”)。不选用另一装置的原因是_________________________________________________________。
(3)若取用样品的质量为2.5 g,收集到气体的体积为280 mL(标准状况),计算样品中Na2O2的质量分数__(写出计算过程)。
【答案】Na2O2样品H2O2Na2O2+2H2O4NaOH+O2↑①过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量78%
【解析】
(1)Na2O2和空气中二氧化碳反应生成Na2CO3,Na2CO3易溶于水但和水不反应,Na2O2和水反应生成NaOH和氧气,所以锥形瓶中应盛Na2O2,分液漏斗中装水;
(2)用托盘天平称量药品时应该遵循“左物右砝”原则,过氧化钠易和空气中水、二氧化碳反应,应该密封称量;
(3)只有Na2O2和水反应生成O2,根据氧气和Na2O2之间的关系式计算Na2O2质量,从而计算其纯度。
(1)Na2O2和空气中二氧化碳反应生成Na2CO3,Na2CO3易溶于水但和水不反应,Na2O2和水反应生成NaOH和氧气,所以锥形瓶中应盛Na2O2,分液漏斗中装水,反应方程式为Na2O2+2H2O=4NaOH+O2↑,故答案为:Na2O2;水;Na2O2+2H2O=4NaOH+O2↑;
(2)用托盘天平称量药品时应该遵循“左物右砝”原则,过氧化钠易和空气中水、二氧化碳反应,应该密封称量,所以选①;不选用另一装置的原因是过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量;
(3)产生O2的物质的量为![]() =0.0125 mol,设过氧化钠的质量为m,
=0.0125 mol,设过氧化钠的质量为m,
2 Na2O2+2H2O=4NaOH+O2↑
2×78g 1 mol
m 0.0125mol
156g:1mol=m:0.0125mol,m=![]() =1.95g,样品中Na2O2的纯度为
=1.95g,样品中Na2O2的纯度为![]() ×100%=78%。
×100%=78%。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案