题目内容
在标准状况下,将1 mol A气体发生如下反应:
2A(g) B(g)+xC(g),达到平衡时,在混合气中A的体积分数为58.6%,混合气的总质量为46 g,密度为1.772 g·L-1。试计算:
B(g)+xC(g),达到平衡时,在混合气中A的体积分数为58.6%,混合气的总质量为46 g,密度为1.772 g·L-1。试计算:
(1)达平衡后,混合气的平均相对分子质量。
(2)达平衡后,A的转化率。
(3)C气体的化学计量数x的数值。
2A(g)
 B(g)+xC(g),达到平衡时,在混合气中A的体积分数为58.6%,混合气的总质量为46 g,密度为1.772 g·L-1。试计算:
B(g)+xC(g),达到平衡时,在混合气中A的体积分数为58.6%,混合气的总质量为46 g,密度为1.772 g·L-1。试计算:(1)达平衡后,混合气的平均相对分子质量。
(2)达平衡后,A的转化率。
(3)C气体的化学计量数x的数值。
(1)39?6(2)32% (3)2
(1)V(混合气)="46" g÷1.772 g·L-1="25.96" L
n(混合气)="1.16" mol
 =
= =39.6
=39.6
(2) 2A B + xC Δn
B + xC Δn
2 x-1
(1-1.16×0.586) mol (1.16-1) mol
x=2
A的转化率为 100%=32%
100%=32%
n(混合气)="1.16" mol
 =
= =39.6
=39.6(2) 2A
 B + xC Δn
B + xC Δn2 x-1
(1-1.16×0.586) mol (1.16-1) mol
x=2
A的转化率为
 100%=32%
100%=32%
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 C(g)+D(g)已达平衡的是___________________________。
C(g)+D(g)已达平衡的是___________________________。 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( ) 2Z(g)。现将X和Y按体积比1∶2混合于一密闭容器中,并加压到3×107 Pa时达到平衡状态。此时反应物、生成物的物质的量之比为6∶1,则此时对应于图28中的温度应为( )
2Z(g)。现将X和Y按体积比1∶2混合于一密闭容器中,并加压到3×107 Pa时达到平衡状态。此时反应物、生成物的物质的量之比为6∶1,则此时对应于图28中的温度应为( )
 (NH3)。
(NH3)。 C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )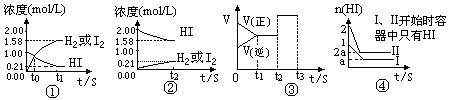
 2SO3中,充入由18O组成的氧气一段时间后,18O存在于下列物质中的( )
2SO3中,充入由18O组成的氧气一段时间后,18O存在于下列物质中的( )