题目内容
8.下列离子方程式正确的是( )| A. | 硝酸银溶液与铜:Cu+Ag+→Cu2++Ag | |
| B. | 氧化铜与盐酸反应:O2-+2H+→H2O | |
| C. | 碳酸钡与盐酸:CO32-+2H+→H2O+CO2↑ | |
| D. | Cu(OH)2加入H2SO4:2H++Cu(OH)2→Cu2++2H2O |
分析 A.离子方程式两边正电荷不相等,违反了电荷守恒;
B.氧化铜为难溶氧化物,离子方程式中不能拆开;
C.碳酸钡为难溶物,离子方程式中应该保留化学式;
D.氢氧化铜与硫酸反应生成硫酸铜和水,氢氧化铜在离子方程式中需要保留化学式.
解答 解:A.铜和硝酸银溶液反应生成银和硝酸铜,正确的离子反应为:Cu+2Ag+=Cu2++2Ag,故A错误;
B.氧化铜与盐酸反应生成氯化铜和水,氧化铜需要保留化学式,正确的离子方程式为:CuO+2H+=Cu2++H2O,故B错误;
C.碳酸钡与盐酸反应生成氯化钡、二氧化碳气体和水,正确的离子反应为:BaCO3+2H+=CO2↑+H2O+Ba2+,故C错误;
D.氢氧化铜与稀硫酸反应生成硫酸铜和水,反应的离子方程式为:2H++Cu(OH)2=Cu2++2H2O,故D正确;
故选D.
点评 题考查离子反应方程式的书写判断,题目难度中等,明确发生的化学反应及离子反应方程式的书写方法即可解答,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
18.下列氧原子的轨道表示式中,能量最低的是( )
| A. | 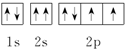 | B. | 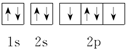 | C. | 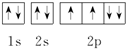 | D. | 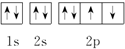 |
19.空气是人类生存所必需的重要资源.为改善空气质量而启动的“蓝天工程”得到了全民的支持.下列措施不利于“蓝天工程”建设的是( )
| A. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 | |
| B. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 实施绿化工程,防治扬尘污染 |
16.下列各组中两种微粒的半径(用r表示)之比小于1的是( )
| A. | $\frac{r(Na)}{r(N{a}^{+})}$ | B. | $\frac{r(S)}{r({S}^{2-})}$ | C. | $\frac{r(Mg)}{r(Al)}$ | D. | $\frac{r(Cl)}{r(F)}$ |
3.下列说法不正确的是( )
| A. | 正常雨水的pH为7.0,酸雨的pH小于7.0 | |
| B. | 严格执行机动车尾气排放标准有利于防止大气污染 | |
| C. | 使用二氧化硫和某些含硫化合物漂白食品会对人体健康产生危害 | |
| D. | PM 2.5是指大气中直径≤2.5微米的颗粒物,戴普通口罩还是对人体健康有影响 |
13.下列做法,不能使CaCO3+2HCl═CaCl2+CO2↑+H2O的反应速率增大的是( )
| A. | 增大盐酸的浓度 | B. | 碾碎碳酸钙 | ||
| C. | 适当加热 | D. | 把盐酸换成同浓度硫酸 |
17.下列各组物质中互为同位素的是( )
| A. | ${\;}_{20}^{40}$Ca和${\;}_{18}^{40}$Ar | B. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | ||
| C. | H2O和H2O2 | D. | O3和O2 |
6.下列关于烷烃与烯烃的性质及反应类型叙述正确的是( )
| A. | 烷烃只含有饱和键,烯烃只含有不饱和键 | |
| B. | 烷烃不能发生加成反应,烯烃不能发生取代反应 | |
| C. | 烷烃不能发生氧化反应,烯烃可以发生氧化反应 | |
| D. | 烷烃与烯烃相比,发生加成反应的一定是烯烃 |
 .
.