题目内容
把4 mol N2和8 mol H2置于5 L密闭容器合成氨反应,经过2min后达到平衡时测得混合气体中含NH3的体积百分比为20%,求:(1)混合气体中含H2的体积百分比;
(2)反应前后容器内的压强比; (3)N2和H2的转化率。(4)求H2的反应速率
(2)反应前后容器内的压强比; (3)N2和H2的转化率。(4)求H2的反应速率
(1)50% (2)6:5 (3) N2的转化率为25%,H2的转化率为37.5%
略

练习册系列答案
相关题目
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则: 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。 装入带活塞的密闭容器中,当反应
装入带活塞的密闭容器中,当反应 达到平衡后,慢慢压缩,下列叙述正确的是
达到平衡后,慢慢压缩,下列叙述正确的是
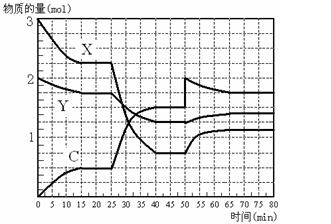
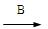 G的离子方程式 。
G的离子方程式 。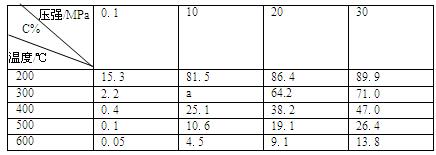

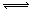 3C(g),已知加入1molA和3molB且达到平衡后,生成amolC。达到平衡后C在反应混和物中的百分含量是
3C(g),已知加入1molA和3molB且达到平衡后,生成amolC。达到平衡后C在反应混和物中的百分含量是 nZ(g)+2W(g)
nZ(g)+2W(g)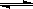 2SO3(g)
2SO3(g) 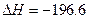 kJ·mol
kJ·mol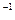 )
) L
L
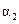
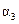
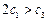 B.
B.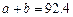 C.
C.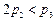 D.
D.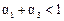
 SO2的转化率为12. 5%,O2的转化率为25%, 开始充入容器中的SO2、O2物质的量之比为4∶1
SO2的转化率为12. 5%,O2的转化率为25%, 开始充入容器中的SO2、O2物质的量之比为4∶1 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。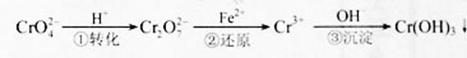

 O
O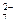
 和CrO
和CrO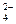 的浓度相同
的浓度相同 ) ="v" (CrO
) ="v" (CrO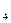 ·7H
·7H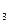 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
 ,要使c(Cr3+)降至10
,要使c(Cr3+)降至10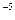 mol/L,溶液的pH应调至 。
mol/L,溶液的pH应调至 。