题目内容
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用.
(1)锌锰干电池是应用最普遍的电池之一(如图1所示),锌锰干电池的负极材料是 , 负极发生的电极反应方程式为: . 若反应消耗32.5g 负极材料,则电池中转移电子的数目为 .
(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O ![]() 2Ni(OH)2+Cd(OH)2 , 已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 . ①以上反应是可逆反应 ②以上反应不是可逆反应
2Ni(OH)2+Cd(OH)2 , 已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 . ①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③
B.②④
C.①④
D.②③
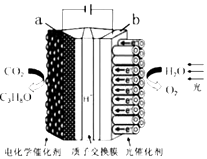
(3)图2为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.则X极为电池的(填“正”或“负”)极,X极的电极反应方程式为
【答案】
(1)锌;Zn﹣2e﹣=Zn2+;NA 或6.02×1023
(2)B
(3)负;CH4+10OH﹣﹣8e﹣=7 H2O+CO ![]()
【解析】解:(1)负极发生氧化反应,锌失电子,电极反应式为:Zn﹣2e﹣=Zn2+ , 32.5g 锌是0.5mol,而1mol的锌失去2mol的电子,所以转移电子的物质的量为1mol,数目为NA 或6.02×1023 , 所以答案是:锌;Zn﹣2e﹣=Zn2+;NA 或6.02×1023;(2)①因为电池冲放电在不同条件下进行,所以该电池反应不是可逆反应,故错误;②因为电池冲放电在不同条件下进行,所以该电池反应不是可逆反应,故正确;③该电池充电时,电能转变为化学能,故错误;④该电池放电时,是将化学能转化为电能,故正确;故选B;(3)电解质溶液为KOH溶液,X电极失去电子,为负极,甲烷被氧化,发生失电子发生氧化反应:CH4﹣8e﹣+10OH﹣═CO ![]() +7H2O,所以答案是:负; CH4+10OH﹣﹣8e﹣=7 H2O+CO
+7H2O,所以答案是:负; CH4+10OH﹣﹣8e﹣=7 H2O+CO ![]() .
.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案