��Ŀ����
6��T��ʱ����1L�ܱ�������A������B���巴Ӧ����C���壮��Ӧ������A��B��CŨ�ȱ仯��ͼI��ʾ�������������������䣬�¶ȷֱ�ΪTl��T2ʱ��B������ٷֺ�����ʱ��Ĺ�ϵ��ͼ����ʾ������������Ϣ��գ�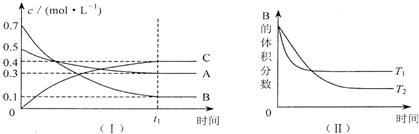
��1����ͼ���֪�÷�Ӧ�Ļ�ѧ����ʽΪA+3B?2C��
��2����ͼ���֪T1��T2���������=�����������������䣬�����¶ȣ���A��ת���ʼ�С����������С�����䣩���������������䣬����ѹǿ����A�����������С����������С�����䣩
��3��T��ʱ������Ӧ��ʼʱA��Ũ��Ϊ0.4mo1•L-1���ﵽƽ������ʵ�Ũ���루������ͬ������ʼʱB��Ũ��Ϊ0.4 mo1•L-1��C��Ũ��Ϊ0.2mo1•L-1���ﵽƽ�����������䣬ͨ��ϡ�����壬ƽ�ⲻ������������ƶ���
���� ��1�����շ�Ӧ��A��B�����ʵ��������Ҳ�Ϊ0�����ڿ��淴Ӧ�������ʵ����仯��֮�ȵ��ڻ�ѧ������֮�ȣ�
��2���¶�Խ�ߣ���Ӧ����Խ�죬����ƽ���ʱ��Խ�̣����¶�T1��T2���������¶ȣ�B�������������˵�������¶�ƽ�������ƶ�������ѹǿ��ƽ�������������С�ķ����ƶ���
��3����ͼ��֪��ƽ��ʱA��Ũ��Ϊ0.3mol/L��B��Ũ��Ϊ0.1mol/L��C��Ũ��Ϊ0.4mol/L����Ӧ��ʼʱA��Ũ��Ϊ0.4mo1•L-1����Ӧ������Ӧ���У�����A��Ũ�ȱ仯�����ٸ��ݷ���ʽ����B��CŨ�ȱ仯������������B��C��ʼŨ�ȣ�
�ﵽƽ������¶�������䣬ͨ��ϡ�����壬�����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���
��� �⣺��1�����շ�Ӧ��A��B�����ʵ��������Ҳ�Ϊ0�����ڿ��淴Ӧ��A��B��C�Ļ�ѧ������֮��Ϊ��0.5-0.3��mol����0.7-0.1��mol��0.4mol=1��3��2���ʷ�Ӧ����ʽΪ��A+3B?2C��
�ʴ�Ϊ��A+3B?2C��
��2����ͼ��֪���¶�T1�ȵ���ƽ�⣬�¶�Խ�ߣ���Ӧ����Խ�죬����ƽ���ʱ��Խ�̣����¶�T1��T2���������¶ȣ�B�������������˵�������¶�ƽ�������ƶ�����A��ת���ʼ�С������ӦΪ���������С�ķ�Ӧ������ѹǿ��ƽ�������ƶ���A�����������С��
�ʴ�Ϊ��������С����С��
��3����ͼ��֪��ƽ��ʱA��Ũ��Ϊ0.3mol/L��B��Ũ��Ϊ0.1mol/L��C��Ũ��Ϊ0.4mol/L����Ӧ��ʼʱA��Ũ��Ϊ0.4mo1•L-1����Ӧ������Ӧ���У�A��Ũ�ȱ仯��Ϊ0.4mol/L-0.3mol/L=0.1mol/L����A+3B?2C ��֪����c��B��=3��c��A��=0.3mol/L����c��C��=2��c��A��=0.2mol/L������ʼʱB��Ũ��Ϊ��0.1+0.3��mo1•L-1=0.4mo1•L-1��C��Ũ��Ϊ ��0.4-0.2��mo1•L-1=0.2mo1•L-1��
�ﵽƽ������¶�������䣬ͨ��ϡ�����壬�����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���
�ʴ�Ϊ��0.4��0.2������
���� ���⿼�黯ѧƽ���йؼ�����Ӱ�����ء���ѧƽ��ͼ���ѶȲ���ע�����á��ȹ���ƽ��ֵ���ж��¶ȸߵͣ�

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�| A�� | �������¶ȣ�X���������������÷�Ӧ�ġ�H��0 | |
| B�� | ���ı�Ӱ��ƽ���һ����������ѧƽ�ⳣ�������仯����ƽ��һ�������ƶ� | |
| C�� | �ı�Ӱ��ƽ���һ��������ƽ�������ƶ�X��ת����һ������ | |
| D�� | �����������䣬�������������Ϊԭ����2����Z��ƽ��Ũ�ȱ�Ϊԭ����$\frac{1}{2}$ |
| A�� | �ֹ� $��_{����}^{Cl_{2}}$ SiCl4$��_{����}^{H_{2}}$Si | |
| B�� | Mg��OH��2$\stackrel{����}{��}$MgCl2��aq��$\stackrel{���}{��}$ Mg�� | |
| C�� | Fe2O3$\stackrel{����}{��}$FeCl3��aq��$\stackrel{����}{��}$��ˮFeCl3 | |
| D�� | AgNO3��aq�� $\stackrel{NH_{3}•H_{2}O}{��}$[Ag��NH3��2]OH��aq�� $��_{��}^{����}$ Ag |
| A�� | ��100mL��Ͳȡ5.0mLϡ���� | |
| B�� | ��������ƽȷ��ȡ2.50gNaCl���� | |
| C�� | ʵ������ȡ����ˮ��װ���У��¶ȼ�ˮ����Ӧ����������ƿҺ������ | |
| D�� | ����240mL0.1mol/LNaOH��ҺӦ��ѡ��250mL������ƿ |
| A�� | ������Һ����μ�����������Һ | |
| B�� | �������Һ����μ���Ũ���� | |
| C�� | �����������Һ��ϡ�����ϣ���ַ�Ӧ | |
| D�� | ����������Һ�еμ����軯����Һ |