题目内容
在温度相同,压强分别为p1和p2的条件下,发生反应:
A(气)+2B(气)![]() nC(气)
nC(气)
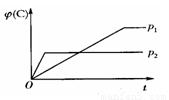
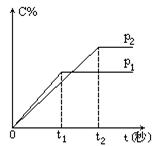
式中C的百分含量与时间t的曲线如下图所示。下面的结论正确的是
A.p1>p2 n<3
B.p1<p2 n>3
C.p1<p2 n=3
D.p1>p2 n>3
D
解析:
从两个曲线可看到,达平衡所需要的时间是p1比p2所需的时间少,因为t1<t2压强增大(即浓度增大),反应速度也变大,所以p1大于p2。故B、C错误。
由平衡时的C%来看,p2时的值大于p1时的值。即在p2时比在p1时更有利于C的生成。由于p1>p2,说明上式的正反应为气体体积增大的反应。这就表明n值应大于1+2。故D正确。

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
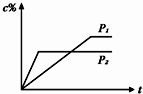 在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g)?n C(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是( )
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g)?n C(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是( ) nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是
nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是
 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是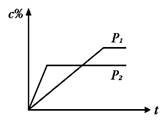
 nC(g)的反应体系中,C的百分含量与时间t的曲线如图所示,下列结论正确的是( )
nC(g)的反应体系中,C的百分含量与时间t的曲线如图所示,下列结论正确的是( )