题目内容
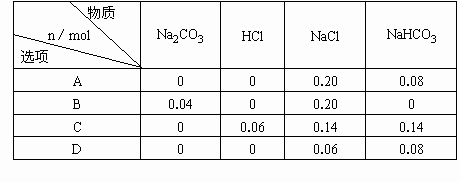
向含0.14mol Na2CO3的溶液中逐滴加入含一定量HCl的稀盐酸,经充分反应后,溶液中各溶质的物质的量判断可能正确的是( )
| A.得0.20molNaCl和0.08molNaHCO3 |
| B.剩0.04molNa2CO3,得0.20molNaCl |
| C.剩0.06molHCl,得0.14molNaCl和0.14molNaHCO3 |
| D.得0.06molNaCl和0.08molNaHCO3 |
Na2CO3与稀盐酸反应要分布进行,Na2CO3+HCl=NaHCO3+NaCl…NaHCO3+HCl=NaCl+CO2↑+H2O,所以溶质的成分可能为:
①Na2CO3、NaHCO3、NaCl
②NaHCO3、NaCl
③NaCl、HCl
所以B、C错误;
又因根据钠元素守恒,0.14mol是Na2CO3,那Na+是0.28mol,A中的钠离子的摩尔数之和刚好为0.28mol,所以A正确;而D中的钠离子的摩尔数之和为0.14mol,所以D错误;
故选:A.
①Na2CO3、NaHCO3、NaCl
②NaHCO3、NaCl
③NaCl、HCl
所以B、C错误;
又因根据钠元素守恒,0.14mol是Na2CO3,那Na+是0.28mol,A中的钠离子的摩尔数之和刚好为0.28mol,所以A正确;而D中的钠离子的摩尔数之和为0.14mol,所以D错误;
故选:A.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目