题目内容
19.0 g Na2CO3和NaHCO3的混合物与足量HCl(aq)反应,得到标准状况下的CO2气体4.48 L。试求:(1)混合物中各成分的质量。
(2)如果HCl(aq)的浓度为0.500 mol·L-1,则所需HCl(aq)的体积至少是多少?
解析:发生的反应有:Na2CO3+2HCl![]() 2NaCl+H2O+CO2↑,
2NaCl+H2O+CO2↑,
NaHCO3+HCl![]() NaCl+H2O+CO2↑。设n(Na2CO3)=x,n(NaHCO3)=y,则
NaCl+H2O+CO2↑。设n(Na2CO3)=x,n(NaHCO3)=y,则
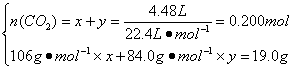
解得:x=0.100 mol,y=0.100 mol
(1)m(Na2CO3)=0.100 mol×106 g·mol-1=10.6 g
m(NaHCO3)=0.100 mol×84.0 g·mol-1=8.40 g
〔或m(NaHCO3)=19.0 g-10.6 g=8.4 g〕
(2)n(HCl)=2x+y=2×0.100 mol+0.100 mol=0.300 mol,
V〔HCl(aq)〕=![]() =0.600 L
=0.600 L
答案:(1)Na2CO3为10.6 g,NaHCO3为8.40 g(或8.4 g) (2)600 mL

练习册系列答案
相关题目