题目内容
今年5月12日14时28分,我国四川省汶川发生特大地震,给人民的生产生活带来了巨大灾难.过氧乙酸(CH3COOOH)是震区防疫消毒广为使用的消毒剂.它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2.测定产品中过氧乙酸浓度c1,涉及下列反应:
①__MnO4-+__H2O2+__H+═__Mn2++__O2+__H2O
②H2O2+2I-+2H+═I2+2H2O
③CH3COOOH+2I-+2H+═CH3COOH+I2+H2O
④I2+2S2O32-═2I-+S4O62-
请回答以下问题:
(1)配平反应①的离子方程式并标出电子转移情况:
______MnO4-+______H2O2+______H+═______Mn2++______O2+______H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是______.
(3)取b0mL待测液,用硫酸使溶液酸化,再用浓度为a1mol?L-1的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1mL(反应①,滴定过程中KMnO4不与过氧乙酸反应).另取b0mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③).再用浓度为a2mol?L-1的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2mL.
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示).c0=______.
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果______(填是或否).
解:(1)在化学反应中,锰元素化合价从+7价降为+2价,共降低5价,双氧水中的氧元素化合价从-1价升高到0价,共升高了2价,化合价升高值和降低值相等,所以高锰酸根之前是2,双氧水之前是5,根据原子守恒和电荷守恒来确定其他的系数,结果为:2MnO4-+5H2O2+6H+═2Mn2++5O2+8H2O,故答案为:2;5;6;2;5;8;
(2)淀粉遇碘单质显蓝色,用Na2S2O3标准溶液滴定I2时可以选用指示剂淀粉溶液,当滴入最后一滴时,溶液的蓝色消失,并且半分钟不变即为滴定终点,故答案为:淀粉溶液;
(3)根据反应I2+2S2O32-═2I-+S4O62-可知,过氧乙酸和残留的H2O2跟KI反应生成I2的总量是: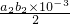 mol,根据反应2MnO4-+5H2O2+6H+═2Mn2++5O2+8H2O,结合高锰酸钾的物质的量可以计算双氧水的物质的量为
mol,根据反应2MnO4-+5H2O2+6H+═2Mn2++5O2+8H2O,结合高锰酸钾的物质的量可以计算双氧水的物质的量为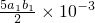 mol,根据反应H2O2+2I-+2H+═I2+2H2O可以知道双氧水氧化碘离子生成碘单质的物质的量为
mol,根据反应H2O2+2I-+2H+═I2+2H2O可以知道双氧水氧化碘离子生成碘单质的物质的量为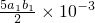 mol,所以过氧乙酸氧化碘离子生成碘单质的物质的量为:(
mol,所以过氧乙酸氧化碘离子生成碘单质的物质的量为:(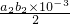 -
-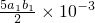 )mol,根据反应CH3COOOH+2I-+2H+═CH3COOH+I2+H2 O知过氧乙酸的物质的量为(
)mol,根据反应CH3COOOH+2I-+2H+═CH3COOH+I2+H2 O知过氧乙酸的物质的量为(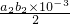 -
-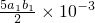 )mol,其浓度为
)mol,其浓度为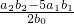 ,
,
故答案为: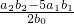 ;
;
(4)根据(3)的计算可以表明计算待测液中过氧乙酸的浓度c0与加入的KI的质量多少没有关系,故答案为:否.
分析:(1)氧化还原反应中化合价升高值=化合价降低值=转移电子数,根据电子守恒来配平方程式;
(2)淀粉遇到单质碘变蓝色,可以用来检验碘单质的生成或存在;
(3)根据物质间的反应结合关系式来计算回答;
(4)过氧乙酸的量和碘单质的量有关,为保证所有的过氧乙酸全反应,必须让碘化钾过量,根据得到单质碘的量来确定过氧乙酸的量.
点评:本题是一道有关氧化还原反应的综合题,考查角度广,要求学生具有分析和解决问题的能力,难度较大.
(2)淀粉遇碘单质显蓝色,用Na2S2O3标准溶液滴定I2时可以选用指示剂淀粉溶液,当滴入最后一滴时,溶液的蓝色消失,并且半分钟不变即为滴定终点,故答案为:淀粉溶液;
(3)根据反应I2+2S2O32-═2I-+S4O62-可知,过氧乙酸和残留的H2O2跟KI反应生成I2的总量是:
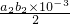 mol,根据反应2MnO4-+5H2O2+6H+═2Mn2++5O2+8H2O,结合高锰酸钾的物质的量可以计算双氧水的物质的量为
mol,根据反应2MnO4-+5H2O2+6H+═2Mn2++5O2+8H2O,结合高锰酸钾的物质的量可以计算双氧水的物质的量为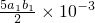 mol,根据反应H2O2+2I-+2H+═I2+2H2O可以知道双氧水氧化碘离子生成碘单质的物质的量为
mol,根据反应H2O2+2I-+2H+═I2+2H2O可以知道双氧水氧化碘离子生成碘单质的物质的量为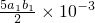 mol,所以过氧乙酸氧化碘离子生成碘单质的物质的量为:(
mol,所以过氧乙酸氧化碘离子生成碘单质的物质的量为:(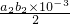 -
-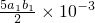 )mol,根据反应CH3COOOH+2I-+2H+═CH3COOH+I2+H2 O知过氧乙酸的物质的量为(
)mol,根据反应CH3COOOH+2I-+2H+═CH3COOH+I2+H2 O知过氧乙酸的物质的量为(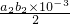 -
-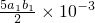 )mol,其浓度为
)mol,其浓度为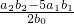 ,
,故答案为:
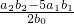 ;
;(4)根据(3)的计算可以表明计算待测液中过氧乙酸的浓度c0与加入的KI的质量多少没有关系,故答案为:否.
分析:(1)氧化还原反应中化合价升高值=化合价降低值=转移电子数,根据电子守恒来配平方程式;
(2)淀粉遇到单质碘变蓝色,可以用来检验碘单质的生成或存在;
(3)根据物质间的反应结合关系式来计算回答;
(4)过氧乙酸的量和碘单质的量有关,为保证所有的过氧乙酸全反应,必须让碘化钾过量,根据得到单质碘的量来确定过氧乙酸的量.
点评:本题是一道有关氧化还原反应的综合题,考查角度广,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
相关题目