题目内容
25 ℃时,浓度均为0.2 mol·L-1的NaHCO3与Na2CO3溶液中,下列判断不正确的是( )
| A.均存在电离平衡和水解平衡 | B.存在的粒子种类相同 |
| C.c(H+)前者小于后者 | D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大 |
C
解析试题分析:A.都存在着水的电离平衡和HCO3-及CO32-的水解平衡。正确。B.在这两种溶液中都存在着Na+、H+、HCO3-、CO32-、OH-、H2CO3、H2O。种类相同。正确。C. HCO3-+ H2O H2CO3+ OH-; HCO3-、CO32-+H2O
H2CO3+ OH-; HCO3-、CO32-+H2O  H2CO3-+OH-.水解程度后者大于前者,所以溶液中C(OH-)浓度CO32-大于HCO3-。因为在溶液中C(H+)·C(OH-)="Kw," C(OH-)越大,C(H+)的浓度就越小。故c(H+) 后者小于前者。错误但符合题意。D.加入NaOH固体,水解平衡CO32-+H2O
H2CO3-+OH-.水解程度后者大于前者,所以溶液中C(OH-)浓度CO32-大于HCO3-。因为在溶液中C(H+)·C(OH-)="Kw," C(OH-)越大,C(H+)的浓度就越小。故c(H+) 后者小于前者。错误但符合题意。D.加入NaOH固体,水解平衡CO32-+H2O  H2CO3-+OH-.逆向移动,c(CO32-)增大。NaHCO3溶液中发生反应NaHCO3+NaOH= Na2CO3+ H2O。c(CO32-)增大。因此c(CO32-)均增大,正确但不符合题意。
H2CO3-+OH-.逆向移动,c(CO32-)增大。NaHCO3溶液中发生反应NaHCO3+NaOH= Na2CO3+ H2O。c(CO32-)增大。因此c(CO32-)均增大,正确但不符合题意。
考点:考查NaHCO3与Na2CO3的化学性质。

25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH—)的变化关系如图所示,则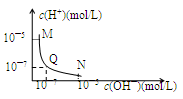
| A.M点所示溶液的导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO―)>c(Na+) |
| C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
| D.M点和N点所示溶液中H2O的电离程度相同 |
常温下,用0.1000mol/LNaOH溶液分别滴定25.00mL0.1000mol/L盐酸溶液和
25.00mL0.1000mol/LCH3COOH溶液,滴定过程中pH变化曲线如下图所示。下列判断不正确的是
| A.滴定盐酸的pH变化曲线为图2 |
| B.在滴定CH3COOH溶液的过程中,始终都有c(Na+)+ c(H+)=c(CH3COO–)+c(OH–) |
| C.滴定CH3COOH溶液的过程中,当滴加12.5mLNaOH溶液时,溶液中离子浓度由大到小的顺序为c(CH3COO–)>c(Na+)>c(H+)>c(OH–) |
| D.当c(Na+)=c(CH3COO–)+ c(CH3COOH)时,溶液的pH<7 |
下列说法不正确的是
| A.Ksp只与难溶电解质的性质和温度有关 |
| B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C.其他条件不变,离子浓度改变时,Ksp不变 |
| D.两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
关于浓度均为0.1 mol·L-1的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
| A.c(NH4+):③>① |
| B.水电离出的c(H+):②>① |
| C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O) |
| D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
关于pH相同的醋酸和盐酸,下列叙述正确的是
| A.取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n |
| B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸 |
| C.取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多 |
| D.两种酸中c (CH3COO-) > c (Cl-) |
物质溶于水的过程中通常伴随着能量的变化,下表为四种物质的溶解热(“+”为放热,“-”为吸热,18℃)
| 化学式 | NH4NO3 | NaOH | Ba(NO3)2 | KNO3 |
| 溶解热(kJ/kg) | –330.75 | +1040.5 | –410.62 | –353.17 |
A.NH4NO3 B.NaOH C.Ba( NO3)2 D.KNO3
常温下,有下列四种溶液:
| ① | ② | ③ | ④ |
| 0.1mol/L NH3·H2O溶液 | pH=11 NaOH溶液 | pH=1 H2SO4溶液 | pH=3 CH3COOH溶液 |
下列说法正确的是( )
A.①与③等体积混合,溶液pH<7
B.②与④等体积混合,溶液pH>7
C.将VmL④的溶液浓缩到10—2VmL后,pH与③相同
D.②与③混合,若溶液pH=7,则V(NaOH) : V(H2SO4) =100 : 1
常温下,下列溶液中的微粒浓度关系正确的是( )
| A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+) >c(OH-)=c(H+) |
| D.0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |