题目内容
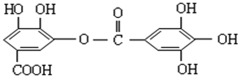
对有机物如图所示的分子叙述不正确的是( )

| A、能发生碱性水解1mol该有机物完全反应消耗8mol氢氧化钠 |
| B、常温下,与碳酸钠溶液反应放出二氧化碳 |
| C、该有机物含有三种官能团 |
| D、与稀硫酸共热反应后混合物中有三种有机物 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知分子式,分子中含酚-OH、-COOH、-COOC-,结合酚、羧酸、酯的性质来解答.
解答:
解:A.酚-OH、-COOH、-COOC-均与NaOH反应,且-COOC-水解生成的酚-OH也与NaOH反应,则1mol该有机物完全反应消耗8molNaOH,故A正确;
B.含有-COOH,酸性比碳酸强,则与碳酸钠溶液反应放出二氧化碳,故B正确;
C.分子中含酚-OH、-COOH、-COOC-三种官能团,故C正确;
D.与稀H2SO4共热,生成一种有机物为 ,故D错误.
,故D错误.
故选D.
B.含有-COOH,酸性比碳酸强,则与碳酸钠溶液反应放出二氧化碳,故B正确;
C.分子中含酚-OH、-COOH、-COOC-三种官能团,故C正确;
D.与稀H2SO4共热,生成一种有机物为
 ,故D错误.
,故D错误.故选D.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重羧酸、酚、酯性质的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室制Cl2反应为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.下列说法不正确的是( )
| ||
| A、氧化剂是MnO2,还原剂是HCl |
| B、每生成1mol Cl2,转移电子的物质的量为2mol |
| C、每消耗1mol MnO2,起还原剂作用的HCl消耗4mol |
| D、转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L |
钛被誉为“21世纪金属”.工业冶炼钛的第一部反应为:TiO2+2C+2Cl2→TiCl4+2CO.下列关于该反应的说法正确的是( )
| A、TiO2是氧化剂 |
| B、氧化剂与还原剂的物质的量之比为1:1 |
| C、Cl2发生氧化反应 |
| D、当2mol C参加反应时,转移电子数目为2mol |
不能达到除杂目的是( )
| A、乙醇(水):加入新制生石灰,蒸馏 |
| B、乙酸乙酯(乙醇):加入NaOH溶液,振荡静置后分液 |
| C、乙酸(乙醇):加入金属钠,蒸馏 |
| D、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
下列物质中,既含有离子键,又含有极性共价键的是( )
| A、NaCl |
| B、NH4NO3 |
| C、Fe2O3 |
| D、Na2O2 |
如图所示装置,电流计的指针发生偏转,正极变粗,负极变细,符合这种情况的是( )
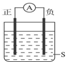

| A、正极Cu,负极Zn,S为稀H2SO4 |
| B、正极Zn,负极Cu,S为CuSO4溶液 |
| C、正极Ag,负极Zn,S为AgNO3溶液 |
| D、正极Fe,负极Cu,S为AgNO3溶液 |