题目内容
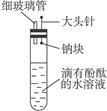
将Na2CO3和NaHCO3的混合物5.48g加热到质量不再减轻时,测得残留固体4.24g。另取一定质量的此混合物固体,跟100mL某浓度的盐酸刚好完全反应,并收集到 672mLCO2气体(标准状况下)求:
(1)此混合物中NaHCO3的质量百分含量;
(2)所用盐酸的物质的量浓度。
(1)此混合物中NaHCO3的质量百分含量;
(2)所用盐酸的物质的量浓度。
(1)61.3%;(2)[HCl]=0.4mol/L
(1)设混合物中含NaHCO3xg
2NaHCO3 Na2CO3+CO2↑+H2O 质量减少
Na2CO3+CO2↑+H2O 质量减少
2×84 106 168-106=62
x 5.48-4.24=1.24
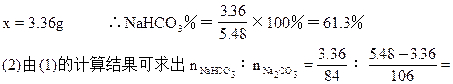
2∶1 则由:
NaHCO3+HCl=NaCl+CO2↑+H2O
2x′ 2x′ 2x′
Na2CO3+2HCl=2NaCl+CO2↑+H2O
x′ 2x′ x′
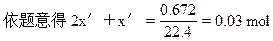
∴x′=0.01mol
故消耗HCl的总的物质的量为4×0.01=0.04 mol盐酸的物质的量
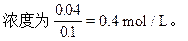
2NaHCO3
 Na2CO3+CO2↑+H2O 质量减少
Na2CO3+CO2↑+H2O 质量减少2×84 106 168-106=62
x 5.48-4.24=1.24
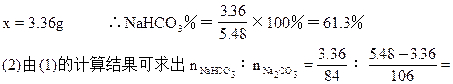
2∶1 则由:
NaHCO3+HCl=NaCl+CO2↑+H2O
2x′ 2x′ 2x′
Na2CO3+2HCl=2NaCl+CO2↑+H2O
x′ 2x′ x′
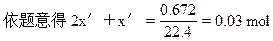
∴x′=0.01mol
故消耗HCl的总的物质的量为4×0.01=0.04 mol盐酸的物质的量
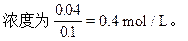

练习册系列答案
相关题目