��Ŀ����
����Ŀ�����ݷ�ӦFe+H2SO4=FeSO4+H2�����ش��������⣮
��1���ڴ˷�Ӧ�У��Է�Ӧ��ʼ��2����ĩ��H2SO4Ũ����1mol/L��Ϊ0.4mol/L����H2SO4�ķ�Ӧ����Ϊ ��
��Ҫʹ�÷�Ӧ�ķ�Ӧ���ʼӿ죬���д�ʩ�����е���������ĸ��
a������ƬΪ���� b����ϡH2SO4Ϊ98%��ŨH2SO4
c�������¶� d���μ�����CuSO4��Һ
��2���ڴ��������ͼ�У������˷�Ӧ��������ϵ�������仯ͼ�����б�Ҫ�ı�ע��
��3�����ݴ˷�Ӧ���һ��ԭ��أ�Ҫ��װ��ͼ�����б�Ҫ�ı�ע ��
���𰸡�
��1��0.3mol/��L?min����b
��2��
��3��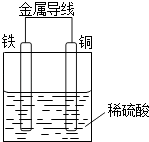
���������⣺��1��v= ![]() =
= ![]() =0.3mol/��Lmin����
=0.3mol/��Lmin����
a������ƬΪ���ۣ����ӽӴ��������Ӧ���ʼӿ죬�ʲ�ѡ��
b����ϡH2SO4Ϊ98%��ŨH2SO4 �� �����ۻ�����Ӧ���ʼ�������ѡ��
c�������¶ȣ���Ӧ���ʼӿ죬�ʲ�ѡ��
d���μ�����CuSO4��Һ������ԭ��ؼӿ췴Ӧ���ʣ��ʲ�ѡ��
��ѡ��0.3mol/��Lmin����b��
��2.����ӦFe+H2SO4=FeSO4+H2�����Ƿ��ȷ�Ӧ�����Է�Ӧ���������������������������������ϵ�������仯ͼΪ��  �����Դ��ǣ�
�����Դ��ǣ�  ��
��
��3.������ԭ��صĸ������������Һ�����ᣬԭ��ص�װ��ͼΪ��  �����Դ��ǣ�
�����Դ��ǣ�  ��
��



