题目内容
[2012·江西省重点中学盟校高三第二次联考理科综合能力测试]在过量的稀硫酸溶液中加入5.6 g Fe粉,待反应完全后,再加入50 mL0.5mol·L-1 KNO3溶液,恰好反应完全。该反应的方程式为:
“ FeSO4 + KNO3 + H2SO4= K2SO4 + Fe2(SO4)3+ NxOy + H2O”,则对该反应的下列说法正确的是( )
A.反应中还原产物是NO
B.氧化产物和还原产物的物质的量之比为1∶4
C.反应过程中转移的电子数为8e-
D.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5
D
【解析】设还原产物中N的化合价为a,由电子守恒可得,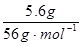 ×1=0.5mol·L-1×50×10-3L×(5-a),解得a=1,所以还原产物为N2O;由得失电子守恒和原子守恒配平化学方程式得8FeSO4 +2KNO3
+5H2SO4=K2SO4 +4Fe2(SO4)3+N2O+5
H2O,由化学方程式可知氧化产物和还原产物的物质的量之比为4∶1,反应过程中转移的电子数为0.1×6.02×1023。
×1=0.5mol·L-1×50×10-3L×(5-a),解得a=1,所以还原产物为N2O;由得失电子守恒和原子守恒配平化学方程式得8FeSO4 +2KNO3
+5H2SO4=K2SO4 +4Fe2(SO4)3+N2O+5
H2O,由化学方程式可知氧化产物和还原产物的物质的量之比为4∶1,反应过程中转移的电子数为0.1×6.02×1023。

[2012·江西省重点中学协作体高三第二次联考]某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是( )
| A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| D.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
[2012·江西省重点中学盟校高三第二次联考理科综合能力测试]在过量的稀硫酸溶液中加入5.6 g Fe粉,待反应完全后,再加入50 mL0.5mol·L-1 KNO3溶液,恰好反应完全。该反应的方程式为:
“ FeSO4 + KNO3 + H2SO4= K2SO4 + Fe2(SO4)3+ NxOy + H2O”,则对该反应的下列说法正确的是( )
| A.反应中还原产物是NO |
| B.氧化产物和还原产物的物质的量之比为1∶4 |
| C.反应过程中转移的电子数为8e- |
| D.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |