题目内容
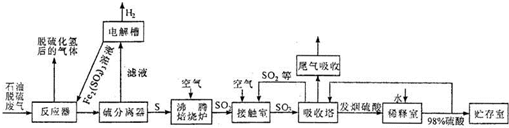
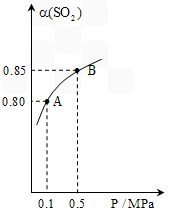
在硫酸工业生产中,SO3的吸收过程是在吸收塔(如右图)中进行的,吸收塔里还装入大量瓷环。下列有关说法中,不正确的是

- A.从①处通入含SO3的混合气体,整个吸收操作采取逆流的形式
- B.从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积
- C.从③处导出的尾气中含量最高的气体是SO2,所以不可直接排入大气
- D.从④处流出的是可用水或稀硫酸稀释的“发烟”硫酸
C
在硫酸工业生产中,为了使SO3的吸收充分,采取逆流的形式,A正确;在吸收塔中装有瓷环,其目的是增大浓硫酸与SO3的接触面积,使SO3尽可能被浓硫酸吸收,B正确,从③处导出的尾气中含量最高的气体是N2,同时还含有未反应完全的SO2、SO3、O2等气体,所以不可直接排入大气中,C错;SO3被浓硫酸吸收后,硫酸成为“发烟硫酸”,此时的“烟”实际上是雾,硫酸小液滴,但是习惯上人们将其称为“烟”,D正确。
在硫酸工业生产中,为了使SO3的吸收充分,采取逆流的形式,A正确;在吸收塔中装有瓷环,其目的是增大浓硫酸与SO3的接触面积,使SO3尽可能被浓硫酸吸收,B正确,从③处导出的尾气中含量最高的气体是N2,同时还含有未反应完全的SO2、SO3、O2等气体,所以不可直接排入大气中,C错;SO3被浓硫酸吸收后,硫酸成为“发烟硫酸”,此时的“烟”实际上是雾,硫酸小液滴,但是习惯上人们将其称为“烟”,D正确。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 (2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
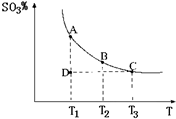
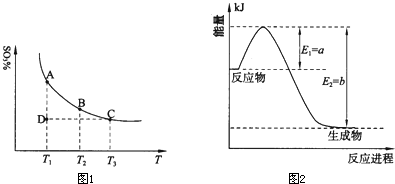
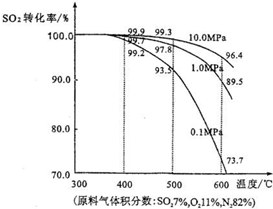
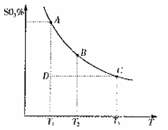
(2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义. 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题: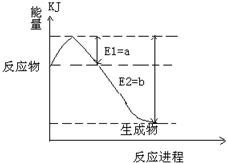

 ①
①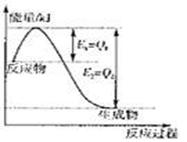 (2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。