题目内容
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3 (aq)+S(s)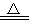 Na2S2O3 (aq)
Na2S2O3 (aq)
实验步骤:
① 称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。 另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
② 安装实验装置(如图所示,部分夹持装置略去),水浴加热, 微沸60分钟。

③ 趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、低温干燥,得到产品。
回答问题:
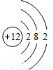
(1) Na2S2O3 中硫元素的化合价为_____________;Na2S2O3在强酸性溶液中不能稳定存在,其原因为___________________(用离子方程式表示)。
(2)仪器a的名称是________,其作用是________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是________。检验其是否存在的方法是___________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂, 用0.100 0 mol·L-1碘的标准溶液滴定(反应原理为:2S2O +I2===S4O
+I2===S4O +2I-)。
+2I-)。
(4)滴定至终点时,溶液颜色的变化:_____________。
(5)滴定结束后消耗碘的标准溶液体积为20.00mL。产品的纯度为(用含W的代数式表示)_____________。
实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和下表中提供的物质完成相关实验,其中合理的选项是
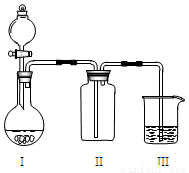
选项 | I中的物质 | II中收集的气体 | III中的物质 |
A | Cu和浓硝酸 | NO | NaOH溶液 |
B | 浓盐酸和高锰酸钾 | Cl2 | NaOH溶液 |
C | 大理石和稀硫酸 | CO2 | 澄清石灰水 |
D | 浓氨水和CaO | NH3 | 滴加酚酞的水 |
下列实验中对应的现象以及结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A | 用洁净铂丝蘸取少量待测液在酒精灯火焰上灼烧 | 火焰呈现黄色 | 待测液中只含Na+,不含K+ |
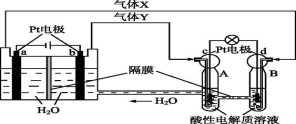
B | 用铁作电极电解饱和食盐水 | 两极上均产生气体 | 阴、阳极分别生成H2和Cl2 |
C | 向饱和氯水中加人少量石灰石 | 产生无色气体 | 酸性:HClO>H2CO3 |
D | 向Ba(ClO)2溶液中 通入足量的SO2 | 产生不溶于稀盐酸的白色沉淀 | Ba(C1O)2具有氧化性 |


 CO3(s)═NH4HCO3(s)+NH3(g)
CO3(s)═NH4HCO3(s)+NH3(g) 生成FeCl3时转移电子数为3NA
生成FeCl3时转移电子数为3NA
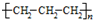
 Cl
Cl