题目内容
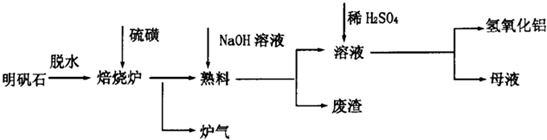
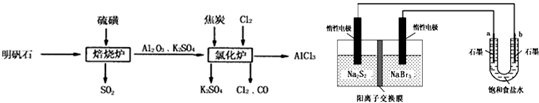
(2013?四川)明矾石经处理后得到明矾[KAl(SO4)2?12H2O].从明矾制备Al、K2SO4、和H2SO4的工艺过程如图1所示:焙烧明矾的化学方程式为:4KAl(SO4)2?12H2O+3S═2K2SO4+2Al2O3+9SO2+48H2O

请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是
(2)从水浸后的滤液中得到K2SO4晶体的方法是
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图2所示,该晶体中Al的配位数是
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是
(5)焙烧产生的SO2可用于制硫酸.已知25℃、101kPa时:
2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;
H2O(g)?H2O(l)△H2=-44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4△H3=-545kJ/mol.
则SO3(g)与H2O(l)反应的热化学方程式是
焙烧948t明矾(M=474g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸

请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是
S
S
.(2)从水浸后的滤液中得到K2SO4晶体的方法是
蒸发结晶
蒸发结晶
.(3)Al2O3在一定条件下可制得AlN,其晶体结构如图2所示,该晶体中Al的配位数是
4
4
.(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是
Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2
Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2
.(5)焙烧产生的SO2可用于制硫酸.已知25℃、101kPa时:
2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;
H2O(g)?H2O(l)△H2=-44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4△H3=-545kJ/mol.
则SO3(g)与H2O(l)反应的热化学方程式是
①SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol
①SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol
.焙烧948t明矾(M=474g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸
②432
②432
t.分析:(1)依据化学方程式中元素化合价变化分析判断,元素化合价升高的做还原剂发生氧化反应;
(2)从水浸后的滤液中得到K2SO4晶体的方法是利用硫酸钾溶解度随温度变化,可以利用蒸发溶剂方法结晶析出;
(3)配位化合物中直接和中心原子(或离子)相联系的配位原子的数目;
(4)以Al和NiO(OH)为电极,铝做原电池 负极失电子发生氧化反应,NiO(OH)得到电子发生还原反应,结合原子守恒和电子守恒写出反应化学方程式;
(5)①依据热化学方程式和盖斯定律计算得到;
②依据硫元素守恒计算得到;
(2)从水浸后的滤液中得到K2SO4晶体的方法是利用硫酸钾溶解度随温度变化,可以利用蒸发溶剂方法结晶析出;
(3)配位化合物中直接和中心原子(或离子)相联系的配位原子的数目;
(4)以Al和NiO(OH)为电极,铝做原电池 负极失电子发生氧化反应,NiO(OH)得到电子发生还原反应,结合原子守恒和电子守恒写出反应化学方程式;
(5)①依据热化学方程式和盖斯定律计算得到;
②依据硫元素守恒计算得到;
解答:解;(1)4KAl(SO4)2?12H2O+3S═2K2SO4+2Al2O3+9SO2+48H2O反应硫单质中硫元素化合价升高为+4价.硫酸根离子中硫元素化合价从+6价变化为+4价,复印纸还原剂是硫单质;
故答案为:S;
(2)从水浸后的滤液中得到K2SO4晶体的方法是利用硫酸钾溶解度随温度变化不大,可以利用蒸发溶剂方法结晶析出晶体;
故答案为:蒸发结晶;
(3)依据晶体晶胞结构分析,结合配位数含义可知,镁个铝原子和四个单原子相连,所以铝原子的配位数为4;
故答案为:4;
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,铝做负极失电子在氢氧化钠溶液中生成偏铝酸钠,反应的化学方程式为:
Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2 ;
故答案为:Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2;
(5)①2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;Ⅰ
H2O(g)?H2O(l)△H2=-44kJ/mol;Ⅱ
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJ/mol.Ⅲ
依据盖斯定律Ⅲ-Ⅰ-2×Ⅱ得到:2SO3(g)+2H2O(l)=2H2SO4(l)△H=-260KJ/mol;
即反应的热化学方程式为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
②948 t明矾生成SO2物质的量为4500mol 故生成硫酸的质量m=4500×0.96×98÷0.98=432000Kg=432t.
故答案为:432t;
故答案为:S;
(2)从水浸后的滤液中得到K2SO4晶体的方法是利用硫酸钾溶解度随温度变化不大,可以利用蒸发溶剂方法结晶析出晶体;
故答案为:蒸发结晶;
(3)依据晶体晶胞结构分析,结合配位数含义可知,镁个铝原子和四个单原子相连,所以铝原子的配位数为4;
故答案为:4;
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,铝做负极失电子在氢氧化钠溶液中生成偏铝酸钠,反应的化学方程式为:
Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2 ;
故答案为:Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2;
(5)①2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ/mol;Ⅰ
H2O(g)?H2O(l)△H2=-44kJ/mol;Ⅱ
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJ/mol.Ⅲ
依据盖斯定律Ⅲ-Ⅰ-2×Ⅱ得到:2SO3(g)+2H2O(l)=2H2SO4(l)△H=-260KJ/mol;
即反应的热化学方程式为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130KJ/mol;
②948 t明矾生成SO2物质的量为4500mol 故生成硫酸的质量m=4500×0.96×98÷0.98=432000Kg=432t.
故答案为:432t;
点评:本题考查了氧化还原反应概念分析判断,晶体结构的理解分析,原电池反应的实质应用,热化学方程式和盖斯定律的计算,元素守恒的计算应用,题目难度中等.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目