题目内容
【题目】半导体工业会产生含氨氟酸的废水。完成下列填空:
(1)为了测定某含氢氟酸的废水中HF浓度,量取25.00 mL废水,滴入2~3滴酚酞试液,用0.0100 mol/L标准NaOH溶液滴定,用去26.00 mL。滴定终点的判断方法是_______________________。废水中的c(HF) =_________mol/L。 (精确到 0.0001)
(2)工业上用石灰乳处理含氢氟酸的废水,处理时要控制反应池中呈碱性,目的是_______。
(3)用石灰乳处理含氢氟酸的废水时,会得到含氟底泥(主要含CaF2、CaCO3、CaSO4),含氟底泥可用于制取氟化钙,其生产流程如下:
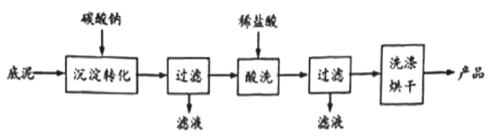
已知:氟化钙难溶于水,微溶于无机酸。
①“沉淀转化”的目的是将CaSO4转化为CaCO3,试从平衡移动的角度分析,沉淀能够转化的原理。____________________________________________________________。
②酸洗是为了除去CaCO3,酸洗时发生反应的离子方程式为______________________。
③最终得到的产品质量比底泥中CaF2的质量__________ (填“多"、“少”或“相等”),理由是____________________________________________________________。
【答案】滴入最后一滴标准液时,溶液由无色变为粉红色且半分钟内不褪色 0.0104 使F-充分沉淀 加入碳酸钠溶液后,碳酸根离子与钙离子结合,转化为溶解度更小的CaCO3沉淀,使CaSO4的沉淀溶解平衡向溶解方向移动 CaCO3+2H+=Ca2++CO2↑+H2O 少 氟化钙微溶于稀盐酸,在酸洗过程中有部分损失
【解析】
(1)滴定终点的判断方法是滴入最后一滴标准液时,溶液由无色变为粉红色且半分钟内不褪色。废水中的c(HF) =![]() =0.0104mol/L;
=0.0104mol/L;
(2)工业上用石灰乳处理含氢氟酸的废水,处理时要控制反应池中呈碱性,目的是使F-充分沉淀;
(3)①“沉淀转化”的目的是将CaSO4转化为CaCO3,加入碳酸钠溶液后,碳酸根离子与钙离子结合,转化为溶解度更小的CaCO3沉淀,使CaSO4的沉淀溶解平衡向溶解方向移动;
②酸洗是为了除去CaCO3,酸洗时碳酸钙溶于酸生成可溶性钙盐,同时生成二氧化碳和水,发生反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O;
③最终得到的产品质量比底泥中CaF2的质量少,理由是氟化钙微溶于稀盐酸,在酸洗过程中有部分损失。

