题目内容
某化肥厂用NH3制备NH4NO3,已知由NH3制NO的产率是96%,NO制HNO3的产率是92%,HNO3与NH3生成NH4NO3均无损失,则制HNO3所用去的氨气的质量占总耗氨质量的质量分数是多少?
53%
解析:设参加反应制HNO3的氨气占总量的质量分数为x,
4NH3+5O2====4NO+6H2O
4×17 4×30
x×96% y
4×17y=4×30×96%x
4NO+3O2+2H2O====4HNO3
4×30 4×63
y·92% z
4×30×z=4×63×92%×y
HNO3+NH3====NH4NO3
63 17
z (1-x)
17z=63(1-x)
所以有(1-x)×63=x×63×92%×96%
x=53%

化学肥料在农业生产中具有重要的作用,关系着农业生产是否丰收。化学肥料在农业生产中的广泛应用,为化学肥料的大规模工业生产提供了舞台。
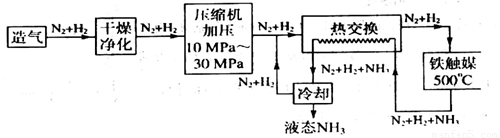
(1)在合成氨的设备(合成塔)中,设置热交换器的目的是______________。
(2)生产硝酸的过程中常会产生一些氮的氧化物,一般可采用下列两种方法处理。
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
氨还原法:8NH3+6NO2 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)
请从绿色化学的角度分析两种方法的优劣:____________________。
(3)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%,NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗用NH3质量(不考虑其他损耗)的________%。
(4)硝酸铵是一种常用的氮肥,在贮存和使用该化肥时,把应注意的事项及理由填入下表(填两条应注意的事项及理由即可)。
|
|
注意事项 |
理由 |
|
① |
______________ |
____________ |
|
② |
________________ |
____________ |