题目内容
【题目】化学电源的发明是化学对人类的一项重大贡献。
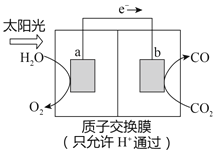
(1)将锌片、铜片按照如图所示装置连接,铜片做__极(填“正”或“负”),外电路电子的流向为__(填“Cu→Zn”或“Zn→Cu”)。

(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为__。
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是__(填序号)。
①NaOH+HCl=NaCl+H2O
②CH4+2O2![]() CO2+2H2O
CO2+2H2O
③Fe+Cu2+=Cu+Fe2+
【答案】正 Zn→Cu Zn+CuSO4=ZnSO4+Cu(Zn+Cu2+=Zn2++Cu) ②③
【解析】
(1)锌片、铜片插入稀硫酸中,由于锌比铜活泼,所以锌做负极,铜做正极,外电路中电子由负极流向正极,即由锌流向铜,故答案为:正;Zn→Cu;
(2)将装置中的稀![]() 用
用![]() 溶液替代,则锌和硫酸铜反应生成硫酸锌和铜,故答案为:Zn+CuSO4=ZnSO4+Cu(Zn+Cu2+=Zn2++Cu);
溶液替代,则锌和硫酸铜反应生成硫酸锌和铜,故答案为:Zn+CuSO4=ZnSO4+Cu(Zn+Cu2+=Zn2++Cu);
(3)能构成原电池的反应是自发进行的氧化还原反应,①![]() 是非氧化还原反应,②CH4+2O2
是非氧化还原反应,②CH4+2O2![]() CO2+2H2O和③Fe+Cu2+=Cu+Fe2+是氧化还原反应,可实现化学能直接转化为电能,故答案为:②③。
CO2+2H2O和③Fe+Cu2+=Cu+Fe2+是氧化还原反应,可实现化学能直接转化为电能,故答案为:②③。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目