题目内容
将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一段时间后,某一电极增重0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化)。此时溶液中氢离子浓度约( )?A.4×10-3mol·L-1 B.2×10-3mol·L-1?
C.1×10-3mol·L-1 D.1×10-7mol·L-1?
解析:(1)电解质溶液中,阳离子在阴极获得的电子数等于阴离子在阳极所释放的电子数。(2)在阳极OH-的放电能力大于SO![]() ,其电极方程式为4OH--4e-
,其电极方程式为4OH--4e-![]() 2H2O+O2↑,再据Cu2++2e-
2H2O+O2↑,再据Cu2++2e-![]() Cu及水的电离反应
Cu及水的电离反应![]() 可得关系式“Cu~2H+”则
可得关系式“Cu~2H+”则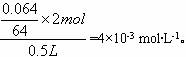
答案:A

练习册系列答案
相关题目