题目内容
某同学设计如图所示的实验装置来粗略测定电石中碳化钙的质量分数。
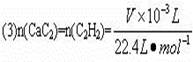
(1)烧瓶中发生反应的化学方程式主要是_________________________________。装置B和C的作用是_______________________________________________。烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了____________________________________________________。
(2)所用的电石质量不能太大,否则____________;也不能太小,否则____________。若容器B的容积为250 mL,则所用的电石质量应在____________g左右(从以下数据选填:0.30、0.60、1.00、1.50、2.00)(气体体积以标准状况计)。
(3)实验中测得排入量筒中水的体积为V mL(以标准状况计),电石质量为m g,则电石中碳化钙质量分数是____________(不计算导管中残留的水,气体中饱和水蒸气也忽略不计)。
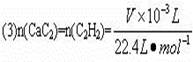
(1)烧瓶中发生反应的化学方程式主要是_________________________________。装置B和C的作用是_______________________________________________。烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了____________________________________________________。
(2)所用的电石质量不能太大,否则____________;也不能太小,否则____________。若容器B的容积为250 mL,则所用的电石质量应在____________g左右(从以下数据选填:0.30、0.60、1.00、1.50、2.00)(气体体积以标准状况计)。
(3)实验中测得排入量筒中水的体积为V mL(以标准状况计),电石质量为m g,则电石中碳化钙质量分数是____________(不计算导管中残留的水,气体中饱和水蒸气也忽略不计)。
(1)CaC2+2H2O→Ca(OH)2+C2H2↑ 测量生成气体的体积 防止气体泄漏
(2)实验失败 误差较大 0.60
(3)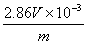
(2)实验失败 误差较大 0.60
(3)
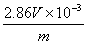
(1)产生的气体进入B,可将B中水排入C,由于V(水)=V(气),所以B、C的作用是测量生成气体的体积。
(2)若电石太大,产生的气体就太多,若V(气)>V(水),则会导致实验失败;若电石太小,产生的气体就太少,就会增大测定误差。V最大(水)="250" mL,n最大(CaC2)=n最小(C2H2)=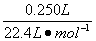 ="0.011" 2 mol,m最大(CaC2)="64.0" g·mol-1×0.011 2 mol="0.717" g。由题意,选用电石的质量可为0.60 g。
="0.011" 2 mol,m最大(CaC2)="64.0" g·mol-1×0.011 2 mol="0.717" g。由题意,选用电石的质量可为0.60 g。
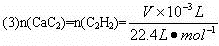
m(CaC2)=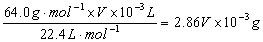
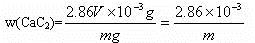
(2)若电石太大,产生的气体就太多,若V(气)>V(水),则会导致实验失败;若电石太小,产生的气体就太少,就会增大测定误差。V最大(水)="250" mL,n最大(CaC2)=n最小(C2H2)=
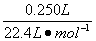 ="0.011" 2 mol,m最大(CaC2)="64.0" g·mol-1×0.011 2 mol="0.717" g。由题意,选用电石的质量可为0.60 g。
="0.011" 2 mol,m最大(CaC2)="64.0" g·mol-1×0.011 2 mol="0.717" g。由题意,选用电石的质量可为0.60 g。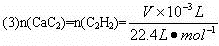
m(CaC2)=
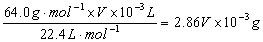
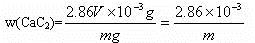

练习册系列答案
相关题目
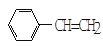 B.
B.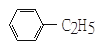 C.
C.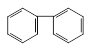 D.
D.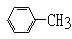
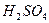 后体积减少30 mL,然后通过碱石灰体积又减少40mL(气体在相同条件下测得)。则这两种烃为( )
后体积减少30 mL,然后通过碱石灰体积又减少40mL(气体在相同条件下测得)。则这两种烃为( ) 与
与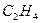
 与
与
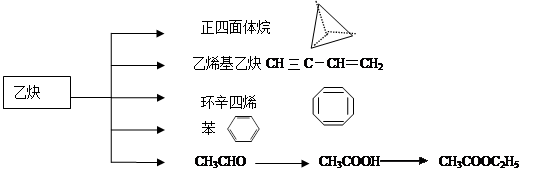
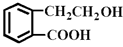 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质: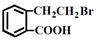 ②
②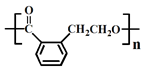 ③
③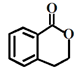 ④
④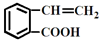
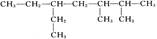 ,则此炔烃可能的结构有( )
,则此炔烃可能的结构有( )