题目内容
下列装置线路接通后,经过一段时间后溶液的pH明显下降的是( )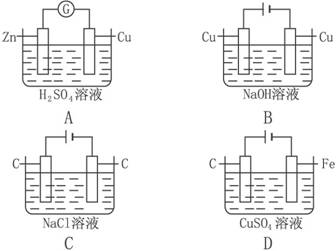
解析:A是原电池,负极为Zn-2e-====Zn2+,正极为2H++2e-====H2↑,总的反应为Zn+2H+====Zn2++H2↑。溶液中c(H+)不断减小,pH升高。B为电解池,且阳极为非惰性电极铜,阳极反应为Cu-2e-====Cu2+,阴极为2H++2e-====H2↑,总的反应为Cu+2H2O====Cu(OH)2↓+H2↑,溶液实际上少了H2O,造成NaOH浓度增大,pH升高。C电解反应式为2Cl-+2H2O====Cl2↑+H2↑+2OH-,pH升高。D电解反应式为2Cu2++2H2O====2Cu+O2↑+4H+,pH变小。
答案:D

练习册系列答案
相关题目

 ” 或“
” 或“ ”表示)、烧杯、灵
”表示)、烧杯、灵 ”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
”表示)和两个电极棒(分别是M、N)进行电化学实验探究。 象回答以下问题:
象回答以下问题: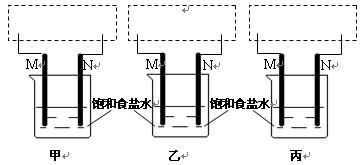
 。
。 ” 或“
” 或“ ”表示)、烧杯、灵
”表示)、烧杯、灵 ”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
