题目内容
(2)质量相同的H2,NH3,SO2,O3四种气体中,含有分子数目最少的是
(3)质量分数为49%的硫酸溶液,其密度为1.8g/cm3,则其物质的量浓度为
(4)在12g某二价金属的硫酸盐中,含量有0.4mol氧原子,此硫酸盐的摩尔质量为
(5)成年男子的肺活量约为3500~4000mL,成年女子的肺活量约为2500~3500mL,肺活量较大的男子与肺活量较小的女子所容纳气体的物质的量之比约为(在同温同压下)
(2)根据N=nNA=
| m |
| M |
| m |
| M |
(3)C=
| 103ρw |
| M |
(4)根据硫酸盐的物质的量与氧原子的物质的量之间的关系式计算硫酸盐的摩尔质量;
(5)相同条件下,气体的物质的量之比等于其体积之比.
(2)根据N=nNA=
| m |
| M |
根据V=
| m |
| M |
故答案为:SO2,H2;
(3)C=
| 103ρw |
| M |
| 103×1.8×49% |
| 98 |
故答案为:9;
(4)1mol某二价金属的硫酸盐中含有4mol氧原子,则含量为0.4mol氧原子的硫酸盐的物质的量是0.1mol,M=
| m |
| n |
| 12g |
| 0.1mol |
(5)相同条件下的气体摩尔体积相同,根据V=nVmZ知,气体的体积之比等于物质的量之比,活量较大的男子与肺活量较小的女子所容纳气体的物质的量之比约为(在同温同压下)=4000:2500=8:5,故答案为:8:5.

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:
已知:
① R1CH=CHR2  R1COOH + R2COOH (R1、R2代表烃基)
R1COOH + R2COOH (R1、R2代表烃基)
 |
②
③C能发生银镜反应,且分子中有支链。
请回答:
(1)E中有 种化学环境不同的H原子,原子个数比是 。
(2)D分子中所含官能团的名称是: 。
(3)写出由一氯环己烷到A的化学方程式: 。
(4)写出满足下列条件的D的一种同分异构体的结构简式 。
①与D具有相同的官能团;②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,则0.1moLH与足量NaOH溶液反应,消耗NaOH moL。
(6)B与E在一定条件下生成F的反应的化学方程式是: 。
有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下: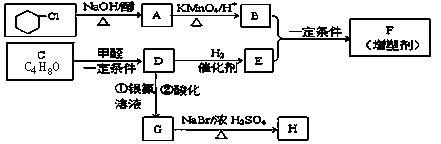
已知:① (R1、R2代表烃基)
(R1、R2代表烃基)
|
 ③C能发生银镜反应,且分子中有支链。
③C能发生银镜反应,且分子中有支链。 请回答:
(1)E中有 种化学环境不同的H原子,原子个数比是 。
(2)D分子中所含官能团的名称是: 。
(3)写出由一氯环己烷到A的化学方程式: 。
(4)写出满足下列条件的D的一种同分异构体的结构简式 。
①与D具有相同的官能团;
②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,则0.1moLH与足量NaOH溶液反应,消耗NaOH
moL。
(6)B与E在一定条件下生成F的反应的化学方程式是: 。
有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:

已知: ① (R1、R2代表烃基)
(R1、R2代表烃基)
|

③C能发生银镜反应,且分子中有支链。
请回答:
(1)E中有 种化学环境不同的H原子,原子个数比是 。
(2)D分子中所含官能团的名称是: 。
(3)写出由一氯环己烷到A的化学方程式: 。
(4)写出满足下列条件的D的一种同分异构体的结构简式 。
①与D具有相同的官能团;
②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,则0.1moLH与足量NaOH溶液反应,消耗NaOH
moL。
(6)B与E在一定条件下生成F的反应的化学方程式是: 。
有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:

已知:
① R1CH=CHR2  R1COOH + R2COOH
(R1、R2代表烃基)
R1COOH + R2COOH
(R1、R2代表烃基)
 |
②
 |
③C能发生银镜反应,且分子中有支链。
请回答:
(1)E中有 种化学环境不同的H原子,原子个数比是 。
(2)D分子中所含官能团的名称是: 。
(3)写出由一氯环己烷到A的化学方程式: 。
(4)写出满足下列条件的D的一种同分异构体的结构简式 。
①与D具有相同的官能团;②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,则0.1moLH与足量NaOH溶液反应,消耗NaOH moL。
(6)B与E在一定条件下生成F的反应的化学方程式是: 。



