题目内容
【题目】亚硝酰氯(NOCl)是一种黄色气体,熔点为-64.5 ℃,沸点为-5.5 ℃,遇水易水解,可用于合成清洁剂、触媒剂等。实验室可由氯气与一氧化氮在常温常压下制备亚硝酰氯。某同学利用纯净的NO和Cl2制备NOCl,装置如下图所示。(已知:Cl2的熔点为-101 ℃,沸点为-34 ℃;NO的熔点为-163.6 ℃,沸点为-151 ℃)
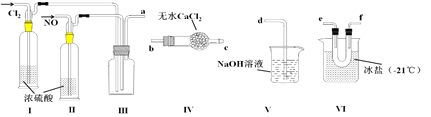
(1)装置连接顺序为a→_______________________(按气流方向,用小写字母表示)。
(2)装置I和II除可进一步干燥NO和Cl2外,另一个作用是____________________。
(3)装置IV的作用是_________________________________,当使用该装置干燥气体时,通常是b口进气,c口出气,原因是__________________________________。
(4)装置V中吸收尾气时,NOCl发生反应的化学方程式为_________________________。
(5)在实际实验操作中,Cl2和NO通入比例略大于1:2,这样做的原因是_________________。
(6)已知王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和一种常见有色气体,该反应的化学方程式为____________________________。
【答案】 e(f)→f(e)→b→c→d 通过观察气泡调节气体流速 防止水蒸气进入VI装置 保证气体和干燥剂充分接触,干燥完全彻底 NOCl+2NaOH=NaCl+NaNO2+H2O 使NO能够完全发生反应,防止NO污染空气 HNO3+3HCl=NOCl↑+Cl2↑+2H2O
【解析】(1)将氯气和NO干燥后在装置Ⅵ中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置,装置连接顺序为a→e(f)→f(e)→b→c→d;
(2)装置I和II除可进一步干燥NO、Cl2外,另一个作用是通过观察气泡调节气体的流速;
(3)NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个装置IV干燥装置防止水蒸气进入反应器;当使用该装置干燥气体时,保证气体和干燥剂充分接触,干燥完全彻底,通常是b口进气,c口出气;
(4)装置 V中吸收尾气时,NOCl发生反应的化学方程式为:NOCl+2NaOH=NaCl+NaNO2+H2O;
(5)NO有毒,对环境有污染,为使NO能够完全发生反应,防止NO污染空气在实际实验操作中,Cl2和NO通入比例略大于1:2;
(6)王水是浓硝酸与浓盐酸按体积比1:3的混酸,一定条件下该混酸可生成亚硝酰氯和Cl2气体,根据电子守恒和原子守恒得该反应的化学方程式为HNO3+3HCl=NOCl↑+Cl2↑+2H2O。

 阅读快车系列答案
阅读快车系列答案