题目内容
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的离子方程式__________。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理___________?并说明理由:________________。
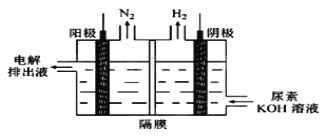
Ⅱ.利用下图装置可以验证非金属性的变化规律。

(3)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置B中所装药品为_____________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(4)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加Na2SiO3,观察到C中的实验现象为有白色沉淀物生成。离子方程式为____________________(假设所通气体是过量的)。
【答案】 2Al+ 6H+ =2Al3+ + 3H2↑ 不合理;用碱性强弱比较金属性强弱时,一定要用元素最高价氧化物对应水化物的碱性强弱比较,NH3·H2O不是N元素最高价氧化物对应的水化物 KMnO4 S2-+Cl2=S↓+2Cl- 硫酸或H2SO4 SiO32- + 2CO2 + 2H2O=H2SiO3↓+ 2HCO3—
【解析】(1)同一周期元素,金属性随着原子序数增大而减弱,元素的金属性越强,同一主族,原子序数越大,金属性越强,其单质与酸或水反应越剧烈,所以金属性K>Na>Mg>Al,则K与盐酸反应最剧烈、Al与盐酸反应速率最慢,反应的离子方程式为2Al+ 6H+=2Al3+ +3H2↑;(2)将NaOH溶液与NH4Cl溶液混合生成NH3H2O,可以说明NaOH的碱性大于NH3H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而NH3H2O不是氮元素的最高价氧化物的水化物;(3)设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO4、Na2S溶液,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为S2-+Cl2=S↓+2Cl-;(4)若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加Na2CO3,故A中可以加硫酸,通过硫酸和碳酸钠的反应来制取CO2,然后的CO2通入C中的Na2SiO3中,可以发生反应:SiO32-+ 2CO2 + 2H2O=H2SiO3↓+ 2HCO3-,产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3,故非金属性:C>Si。

【题目】海水是巨大的资源宝库。下图是实验室模拟工业从海水资源获取某些重要化工原料的流程示意图。

回答下列问题:
(1)由于溴离子在海水中浓度很低(0.067g/L),要进行溴元素的浓缩、富集。实验室若要直接浓缩海水时,下面的仪器肯定不需要的是(填编号)__________
A.玻璃棒 B.三脚架 C.坩埚 D.蒸发皿 E.酒精灯
(2)要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是___________。
A.分析氯化钠含量 B.测定溶液密度 C.观察是否有沉淀析出
(3)写出溴水中通入SO2时反应的离子方程式____________。
(4)上图中虚线框内流程也可用![]() Na2CO3溶液吸收Br2的反应化学方程式补充完整:
Na2CO3溶液吸收Br2的反应化学方程式补充完整:
____Br2 + _____Na2CO3 = _____NaBrO3 +___________ +________
(5)现有一份吸收了溴的无色溶液(采用上述两种方法之一,且吸收剂和溴恰好完全反应),请你通过实验探究该溶液究竟是采用那种方法吸收溴的。
① 提出合理假设
假设1:采用纯碱吸收法,吸收液中含大量Na+、Br –、BrO3-
假设2:_____________________________________________。
② 设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论。限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管;无水乙醇、苯、0.10mol/LAgNO3、0.10mol/LBaCl2、2mol/LHCl 查资料得:Ba(BrO3)2为白色固体,微溶于水
实验步骤 | 预期现象和结论 |
步骤1:用量筒取样品溶液2mL分别于A、B试管中,往A试管中加入___________。 | 若____________________________,则假设1一定能成立。 |
步骤2:往试管B中加入___________。 | 若_________________,则假设2一定能成立。 |