题目内容
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产.主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等。回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)。热化学方程式如下:①C3H6(g)+NH3(g)+ ![]() O2(g)═C3H3N(g)+3H2O(g)△H=﹣515kJmol﹣1 ②C3H6(g)+O2(g)═C3H4O(g)+H2O(g)△H=﹣353kJmol﹣1
O2(g)═C3H3N(g)+3H2O(g)△H=﹣515kJmol﹣1 ②C3H6(g)+O2(g)═C3H4O(g)+H2O(g)△H=﹣353kJmol﹣1
两个反应在热力学上趋势均很大,其原因是;有利于提高丙烯腈平衡产率的反应条件是;提高丙烯腈反应选择性的关键因素是 .
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃.低于460℃时,丙烯腈的产率(填“是”或“不是”)对应温度下的平衡转化率,判断理由是;高于460℃时,丙烯腈产率降低的可能原因是(双选,填标号).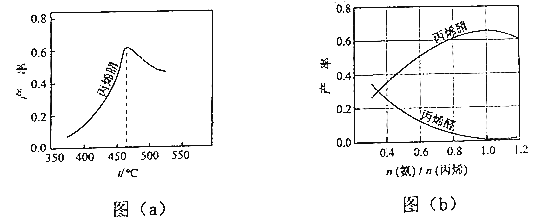
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示.由图可知,最佳n(氨)/n(丙烯)约为 , 理由是 . 进料气氨、空气、丙烯的理论体积比约为 .
【答案】
(1)两个反应均为放热量大的反应,生成产物丙烯晴和丙烯醛均有较稳定的碳碳三键和碳碳双键能量低,故热力学趋势大;低温、低压;催化剂
(2)不是;反应开始进行主要是向正反应方向进行,尚未达到平衡;AC
(3)1:1;此时产物主要是丙烯晴无,副产物几乎无有;1:7.5:1
【解析】(1)两个反应在热力学上趋势均很大,其原因是因为两个反应均为放热量大的反应,生成产物丙烯晴和丙烯醛均有较稳定的碳碳三键和碳碳双键能量低,所以热力学趋势大;该反应为气体体积增大的放热反应,所以降低温度、降低压强有利于提高丙烯腈的平衡产率,由图b可知,提高丙烯腈反应选择性的关键因素是催化剂,
所以答案是:两个反应均为放热量大的反应,生成产物丙烯晴和丙烯醛均有较稳定的碳碳三键和碳碳双键能量低,故热力学趋势大;低温、低压;催化剂;(2)因为该反应为放热反应,平衡产率应随温度升高而降低,反应刚开始进行,尚未达到平衡状态,460°C以前是建立平衡的过程,所以低于460°C时,丙烯腈的产率不是对应温度下的平衡产率;高于460°C时,丙烯腈产率降低,
A.催化剂在一定温度范围内活性较高,若温度过高,活性降低,故A正确;
B.平衡常数的大小不影响产率,故B错误;
C.根据题意,副产物有丙烯醛,副反应增多导致产率下降,故C正确;
D.反应活化能的大小不影响平衡,故D错误;
所以答案是:不是,该反应为放热反应,平衡产率应随温度升高而降低;AC;(3)根据图象可知,当 ![]() 约为1时,该比例下丙烯腈产率最高,而副产物丙烯醛产率最低;根据化学反应C3H6(g)+NH3(g)+
约为1时,该比例下丙烯腈产率最高,而副产物丙烯醛产率最低;根据化学反应C3H6(g)+NH3(g)+ ![]() O2(g)=C3H3N(g)+3H2O(g),氨气、氧气、丙烯按1:1.5:1的体积比加入反应达到最佳状态,而空气中氧气约占20%,所以进料氨、空气、丙烯的理论体积约为:1:7.5:1,
O2(g)=C3H3N(g)+3H2O(g),氨气、氧气、丙烯按1:1.5:1的体积比加入反应达到最佳状态,而空气中氧气约占20%,所以进料氨、空气、丙烯的理论体积约为:1:7.5:1,
所以答案是:1:1;此时产物主要是丙烯晴无,副产物几乎无有;1:7.5:1;
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案