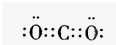题目内容
下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族) .
(2)8个元素的最高价氧化物的水化物中,酸性最强的是 (填化学式).
(3)①元素和⑥元素形成化合物的电子式是 .
(4)写出④最高价氧化物对应水化物与①最高价氧化物对应水化物反应的离子方程式: .
(5)比较半径大小Na+ O2-(填>,=,<=)
(6)下列叙述正确的是 (填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(1)⑧在元素周期表中的位置是(周期、族)
(2)8个元素的最高价氧化物的水化物中,酸性最强的是
(3)①元素和⑥元素形成化合物的电子式是
(4)写出④最高价氧化物对应水化物与①最高价氧化物对应水化物反应的离子方程式:
(5)比较半径大小Na+
(6)下列叙述正确的是
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
分析:这些元素是第二、三周期元素,主族元素的最高化合价与其族序数相等,同一周期元素,原子半径随着原子序数的增大而减小,同一主族元素,原子半径随着原子序数增大而增大,
根据元素化合价结合原子半径知,①是Na元素、②Mg元素、③Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,
根据元素和物质的结构和性质分析解答.
根据元素化合价结合原子半径知,①是Na元素、②Mg元素、③Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,
根据元素和物质的结构和性质分析解答.
解答:解:这些元素是第二、三周期元素,主族元素的最高化合价与其族序数相等,同一周期元素,原子半径随着原子序数的增大而减小,同一主族元素,原子半径随着原子序数增大而增大,
根据元素化合价结合原子半径知,①是Na元素、②Mg元素、③是Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,
(1)⑧是O元素,O原子核外有2个电子层,最外层有6个电子,所以在元素周期表中的位置是(周期、族)第二周期第ⅥA族,
故答案为:第二周期第ⅥA族;
(2)非金属的非金属性越强其最高价含氧酸的酸性越强,但氟元素没有含氧酸,所以非金属元素次之的是Cl元素,8个元素的最高价氧化物的水化物中,酸性最强的是HClO4,
故答案为:HClO4;
(3)①元素和⑥元素形成化合物是氯化钠,氯化钠的电子式是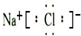 ,
,
故答案为: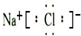 ;
;
(4)④最高价氧化物对应水化物是氢氧化铝,①最高价氧化物对应水化物是氢氧化钠,氢氧化铝和氢氧化钠反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(5)电子层结构相同的离子中,离子半径随着原子序数的增大而减小,所以半径大小:Na+<O2-,
故答案为:<;
(6)A.③是Li元素、④是Al元素,③、④处于不同周期,故正确;
B.②Mg元素,⑧是O元素,②的阳离子与⑧的阴离子的核外电子数相等,都是10个电子,故正确;
C.⑥是Cl元素,F在其同主族元素中非金属性最强,故错误;
D.⑤是P元素、⑦是N元素,二者位于同一主族,所以⑤元素与⑦元素两者核电荷数之差是8,故正确;
E.①是Na元素、⑧是O元素,①与⑧形成的化合物没有两性,故错误;
故选:ABD.
根据元素化合价结合原子半径知,①是Na元素、②Mg元素、③是Li元素、④是Al元素、⑤是P元素、⑥是Cl元素、⑦是N元素、⑧是O元素,
(1)⑧是O元素,O原子核外有2个电子层,最外层有6个电子,所以在元素周期表中的位置是(周期、族)第二周期第ⅥA族,
故答案为:第二周期第ⅥA族;
(2)非金属的非金属性越强其最高价含氧酸的酸性越强,但氟元素没有含氧酸,所以非金属元素次之的是Cl元素,8个元素的最高价氧化物的水化物中,酸性最强的是HClO4,
故答案为:HClO4;
(3)①元素和⑥元素形成化合物是氯化钠,氯化钠的电子式是
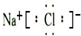 ,
,故答案为:
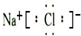 ;
;(4)④最高价氧化物对应水化物是氢氧化铝,①最高价氧化物对应水化物是氢氧化钠,氢氧化铝和氢氧化钠反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(5)电子层结构相同的离子中,离子半径随着原子序数的增大而减小,所以半径大小:Na+<O2-,
故答案为:<;
(6)A.③是Li元素、④是Al元素,③、④处于不同周期,故正确;
B.②Mg元素,⑧是O元素,②的阳离子与⑧的阴离子的核外电子数相等,都是10个电子,故正确;
C.⑥是Cl元素,F在其同主族元素中非金属性最强,故错误;
D.⑤是P元素、⑦是N元素,二者位于同一主族,所以⑤元素与⑦元素两者核电荷数之差是8,故正确;
E.①是Na元素、⑧是O元素,①与⑧形成的化合物没有两性,故错误;
故选:ABD.
点评:本题考查了原子结构和元素周期律的关系,正确推断元素是解本题关键,明确元素周期律的灵活运用,难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目