题目内容
根据下列实验现象得出的结论正确的是
选项????????????? 实验现象????????????? 结论
A????????????? 将BaSO4浸泡在宝盒Na2CO3溶液中,部分BaSO4转化为BaCO3????????????? Ksp(BaSO4)>Ksp(BaCO3)
B????????????? 某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成????????????? 该溶液中一定存在SO42-
C????????????? 滴有酚酞的Na2CO3溶液中加入BaCl2固体,红色变浅????????????? Na2CO3溶液中存在水解平衡
D????????????? 溴水中通入SO2,溴水褪色????????????? SO2具有漂白性
C
【解析】
试题分析:A.BaSO4在水中存在沉淀溶解平衡,BaSO4(s)  Ba2+(aq)+SO42- (aq)。当向水中加入Na2CO3溶液时,若c(Ba2+)·c(CO32-) ≥Ksp(BaCO3)时,就会产生一部分BaCO3 沉淀,促使BaSO4溶解。最终达到平衡时一部分BaSO4转化为BaCO3沉淀。这与二者的溶解度的大小无关。错误。B.若溶液中含有Ag+,加入盐酸酸化的BaCl2溶液时,会产生AgCl不是沉淀,发生上述现象。错误。C. 向滴有酚酞的Na2CO3溶液中加入BaCl2固体时发生沉淀反应Ba2++CO32- = BaCO3↓。由于c(CO32-)减小,其水解产生的c(OH-)减小,溶液的碱性减弱,所以红色变浅。错误。
Ba2+(aq)+SO42- (aq)。当向水中加入Na2CO3溶液时,若c(Ba2+)·c(CO32-) ≥Ksp(BaCO3)时,就会产生一部分BaCO3 沉淀,促使BaSO4溶解。最终达到平衡时一部分BaSO4转化为BaCO3沉淀。这与二者的溶解度的大小无关。错误。B.若溶液中含有Ag+,加入盐酸酸化的BaCl2溶液时,会产生AgCl不是沉淀,发生上述现象。错误。C. 向滴有酚酞的Na2CO3溶液中加入BaCl2固体时发生沉淀反应Ba2++CO32- = BaCO3↓。由于c(CO32-)减小,其水解产生的c(OH-)减小,溶液的碱性减弱,所以红色变浅。错误。
考点:考查

根据下列实验现象得出的结论不正确的是( )
|
根据下列实验现象得出的结论不正确的是
|
|
实验 |
现象 |
结论 |
|
A |
|
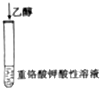
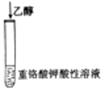
橙色溶液变成绿色 |
乙醇具有还原性 |
|
B |
|
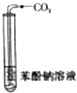
澄清溶液变浑浊 |
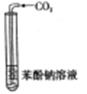
碳酸的酸性比苯酚强 |
|
C |
|
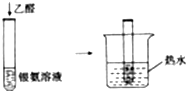
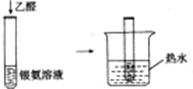
试管内壁有银镜生成 |
乙醛具有还原性 |
|
D |
|
试管中有白色沉淀生成,加水不溶解 |
醋酸铅使蛋白质盐析 |
根据下列实验现象得出的结论不正确的是
| 实验 | 现象 | 结论 | |
| A | 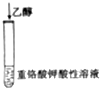 | 橙色溶液变成绿色 | 乙醇具有还原性 |
| B | 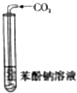 | 澄清溶液变浑浊 | 碳酸的酸性比苯酚强 |
| C | 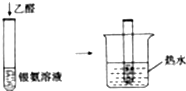 | 试管内壁有银镜生成 | 乙醛具有还原性 |
| D |  | 试管中有白色沉淀生成,加水不溶解 | 醋酸铅使蛋白质盐析 |
- A.A
- B.B
- C.C
- D.D