题目内容
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
- A.Y的低价氧化物与O3漂白的原理相同
- B.Y的氢化物和W2Y所含化学键的类型相同
- C.上述三种元素形成的简单离子,X离子半径最小
- D.工业上常用电解相应的盐溶液制备W、X的单质
C
试题分析:W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水。这说明金属一定有金属铝和钠。根据原子序数大小可知W是Na,X是Al。Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y,所以Y是S元素。A不正确,SO2的漂白原理是化合,而臭氧的漂白是氧化性;H2S中含有共价键,Na2S中含有离子键,B不正确;S2-核外有3个电子层。Na+和Al3+具有2个电子层,离子半径均小于S2-的。在核外电子排布相同的条件下,微粒半径随原子序数的增大而减小,即Al3+离子半径最小,C正确;钠和铝都是活泼的金属,需要电解法冶炼,D不正确,答案选C。
考点:考查元素周期表的结构和元素周期律的应用
点评:该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
试题分析:W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水。这说明金属一定有金属铝和钠。根据原子序数大小可知W是Na,X是Al。Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y,所以Y是S元素。A不正确,SO2的漂白原理是化合,而臭氧的漂白是氧化性;H2S中含有共价键,Na2S中含有离子键,B不正确;S2-核外有3个电子层。Na+和Al3+具有2个电子层,离子半径均小于S2-的。在核外电子排布相同的条件下,微粒半径随原子序数的增大而减小,即Al3+离子半径最小,C正确;钠和铝都是活泼的金属,需要电解法冶炼,D不正确,答案选C。
考点:考查元素周期表的结构和元素周期律的应用
点评:该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
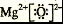
 体类型可能是(填序号)__________。
体类型可能是(填序号)__________。