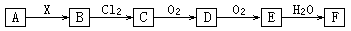题目内容
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②AlCl3、Al(OH)3
③Na、Na2O ④NaOH 、Na2CO3
A.①②③ B.①②
C.③④ D.①②③④
D
解析试题分析:碳和不足量的氧气生成一氧化碳,一氧化碳和氧气继续反映生成二氧化碳;氯化铝和少量的碱性溶液生成氢氧化铝沉淀,氢氧化铝继续和碱性溶液反应生成偏铝酸离子;钠和氧气在空气中什么氧化钠,氧化钠和氧气点燃生成过氧化钠;氢氧化钠和少量碳酸生成碳酸钠,碳酸钠和碳酸生成碳酸氢钠。所以D正确。
考点:化学反应。

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
某研究小组探究:
I .铜片和浓硫酸的反应(夹持装置和A中加热装置已略,气密性已检验)
II. SO2和 Fe( NO3)3溶液的反应[1.0 mol/L的 Fe(NO3)3溶液的 pH=1]请回答下列有关问题:
探究I
(l)某学进行了下列实验:取12.8g铜片和20 mL 18 mol?L-1的浓硫酸放在三颈瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。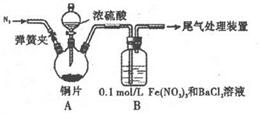
①装置A中反应的化学方程式是_______
②该同学设计求余酸浓度的实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是______ (填字母)。
| A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称貴 |
| B.将产生的气体缓缓通入酸性髙锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀 |
| C.用排水法测定其产生气体的体积(折算成标准状况) |
| D.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况) |
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是______。
(3)裝置B中产生了白色沉淀,分析B中产生白色沉淀的原因,提出下列三种猜想:
猜想1:SO2与Fe3+反应;猜想2 :在酸性条件下SO2与NO3-反应;猜想3:____________;
①按猜想1,装置B中反应的离子方程式是______,证明该猜想应进一步确认生成的新物质,其实验操作及现象是____________。
②按猜想2,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列某种溶液,在相同条件下进行实验。应选择的替换溶液是______ (填序号)。
a.0.1 mol/L 稀硝酸 b. 1.5 mol/L Fe(NO3)2溶液
c. 6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
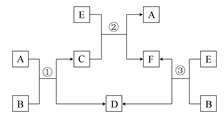
X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是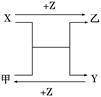
| A.若X为金属单质,Y为非金属固体单质,则Z为O2 |
| B.若X、Y均为金属单质,则甲不可能为黑色固体 |
| C.若X为金属单质,Y为非金属气体单质,则乙可能为黑色固体 |
| D.若X、Y均为非金属固体单质,则Z可能为O2 |
含某元素的物质间能实现如下直接转化,该元素是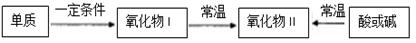
| A.碳 | B.氮 | C.硫 | D.钠 |
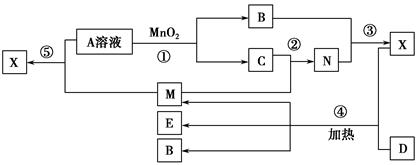
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如图所示。则甲和X不可能是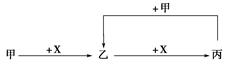
| A.甲为C,X为O2 |
| B.甲为SO2,X为NaOH溶液 |
| C.甲为Fe,X为Cl2 |
| D.甲为AlCl3溶液,X为NaOH溶液 |