题目内容
下列判断中一定正确的是( )
| A.等物质的量的CaCl2及CaO2固体中阴、阳离子数之比均为2∶1 |
| B.等质量的O2与O3中,氧原子的个数比为3∶2 |
| C.分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1∶2 |
| D.10mL 0.3mol·L-1NaCl与30mL0.1mol·L-1AlCl3溶液中Cl-物质的量浓度比为1∶3 |
C
试题分析:A:CaO2中含的阴离子是过氧根O22-,阴阳离子数之比为1:1,故A错;B:氧气与臭氧的摩尔质量数不相同,等质量的氧气与臭氧中氧原子个数比为1:1,故B错;用双氧水制取氧气,制取1mol氧气转移电子数2mol,用高锰酸钾制取氧气,制取1mol氧气转移电子数4mol,所以转移电子数之比为1:2;D:10mL 0.3mol·L-1NaCl与30mL0.1mol·L-1AlCl3溶液中Cl-物质的量浓度比为1∶1,D错,故选C。
点评:A中明确CaO2固体中含有的阴离子是过氧根,而不是两个氧负离子

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
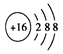
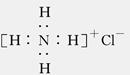
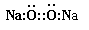
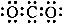


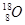
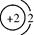
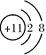
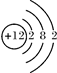

 H3O++ CO32-
H3O++ CO32- H2O+ CO2+2OH-
H2O+ CO2+2OH-