题目内容
【题目】下列数据中合理的是
A.用10 mL量筒量取7.13 mL稀盐酸
B.用托盘天平称量25.20 g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用25 mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70 mL
【答案】D
【解析】
A. 量筒的精确度为0.1ml,A项错误;
B. 托盘天平的精确度为0.1g,B项错误;
C. 广范pH试纸是粗略测量溶液酸碱性的工具,不能测出pH为2.3,C项错误;
D. 滴定管的精确度为0.01ml,用碱式滴定管可以量取21.70ml的碱溶液,D项正确;
答案选D。

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案【题目】环己酮(如图1)是一种重要的化工原料,实验室常用下列原理和装置制备(部分夹持仪器未画出)(如图2):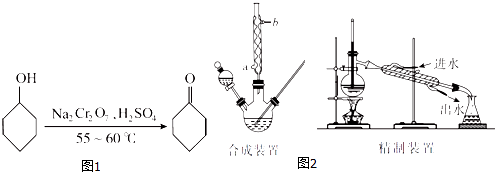
环己醇、环己酮和水的部分物理性质见下表(*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点):
物质 | 相对分子质量 | 沸点(℃) | 密度(gcm﹣3 , 20℃) | 溶解性 |
环己醇 | 100 | 161.1(97.8) | 0.9624 | 能溶于水 |
环己酮 | 98 | 155.6(95) | 0.9478 | 微溶于水 |
水 | 18 | 100.0 | 0.9982 |
(1)已知合成环己酮的反应是放热反应,反应剧烈将导致体系温度迅速上升,副反应增多.实验时,先在合成装置中加入5.2 mL(5 g)环己醇和几粒沸石,再加入酸性Na2Cr2O7溶液.酸性Na2Cr2O7溶液的加料方式为(填代号).
A.一次性加入
B.缓慢加入
C.无所谓,怎样加入都可以
(2)若酸性Na2Cr2O7溶液的体积为35 mL,则应选取(填“100 mL”或“250mL”)的三颈瓶.
(3)反应完成后,加入适量水,蒸馏,收集95~100℃的馏分(设为A),其主要成分是的混合物.
(4)合成装置中冷凝管的作用是 , 冷凝水从冷凝管的(填“a”或“b”)口进入.
(5)在馏分A中加入氯化钠固体至饱和,振荡、静置、分液,得有机层(设为B).加入氯化钠固体的作用是 .
(6)在有机层B中加入无水硫酸镁固体,除去其中的少量水分.过滤,将滤液置于精制装置中蒸馏,收集(填代号)的馏分,得到纯净的环己酮.
A.100.0~102.0℃
B.154.0~156.0℃
C.160.0~162.0℃
(7)精制装置中的错误是 . (任写一点)
(8)若最终得到环己酮的质量为3.43 g,则环己酮的产率是 .