题目内容
设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一.最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生反应的化学方程式是
(2)这个电池负极发生的反应是:C4H10+13O2--26e-=4CO2+5H2O,正极发生的电极反应方程式是:
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
(4)汽油燃料电池最大的障碍是氧化反应不完全产生
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生反应的化学方程式是
2C4H10+13O2═8CO2+10H2O
2C4H10+13O2═8CO2+10H2O
;(2)这个电池负极发生的反应是:C4H10+13O2--26e-=4CO2+5H2O,正极发生的电极反应方程式是:
O2+4e-=2O2-
O2+4e-=2O2-
;固体电解质里O2-向负
负
极移动; 向外电路释放的电子的电极是负
负
极;(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
燃料电池具有较高的能量利用率
燃料电池具有较高的能量利用率
;(4)汽油燃料电池最大的障碍是氧化反应不完全产生
碳粒或C
碳粒或C
堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年,这正是新一代化学家的历史使命.分析:(1)燃料电池的总反应和燃料燃烧的化学方程式一致;
(2)正极发生还原反应,总反应减负极反应可得正极反应式;原电池工作时,阴离子向负极移动,电子从负极经外电路流向正极;
(3)原电池具有能量利用率高的特点;
(4)丁烷不完全氧化会生成碳粒,从而堵塞电极的气体通道.
(2)正极发生还原反应,总反应减负极反应可得正极反应式;原电池工作时,阴离子向负极移动,电子从负极经外电路流向正极;
(3)原电池具有能量利用率高的特点;
(4)丁烷不完全氧化会生成碳粒,从而堵塞电极的气体通道.
解答:解:(1)燃料电池的总反应和燃料燃烧的化学方程式一致,电池总反应为2C4H10+13O2═8CO2+10H2O,
故答案为:2C4H10+13O2═8CO2+10H2O;
(2)极发生还原反应,总反应减负极反应可得正极反应式,为O2+4e-=2O2-;原电池工作时,阴离子向负极移动,电子从负极经外电路流向正极故答案为:O2+4e-=2O2-; 负; 负;
(3)原电池具有能量利用率高的特点,而燃烧时化学能转变为热能和光能,
故答案为:燃料电池具有较高的能量利用率;
(4)烷不完全氧化会生成碳粒,从而堵塞电极的气体通道,故答案为:碳粒或C.
故答案为:2C4H10+13O2═8CO2+10H2O;
(2)极发生还原反应,总反应减负极反应可得正极反应式,为O2+4e-=2O2-;原电池工作时,阴离子向负极移动,电子从负极经外电路流向正极故答案为:O2+4e-=2O2-; 负; 负;
(3)原电池具有能量利用率高的特点,而燃烧时化学能转变为热能和光能,
故答案为:燃料电池具有较高的能量利用率;
(4)烷不完全氧化会生成碳粒,从而堵塞电极的气体通道,故答案为:碳粒或C.
点评:本题考查化学电源新型电池,题目难度中等,注意电极反应式的书写.

练习册系列答案
相关题目
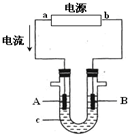 Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.