题目内容
 看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)(1)如果在虚线部分增加收集装置,上图中装置可用于实验室制取氨气,请回答以下问题:
①可以用
瓶口向下排空气法
瓶口向下排空气法
方法收集氨气,如果用烧瓶收集氨气,请用文字叙述如何检验氨气己收集满用湿润的红色石蕊试纸靠近瓶口,试纸变蓝,说明已收集满
用湿润的红色石蕊试纸靠近瓶口,试纸变蓝,说明已收集满
;②利用①中收集的氨气可以完成喷泉实验,是因为氨气具有
极易溶于水
极易溶于水
的物理性质;③写出实验室制氨气的化学反应方程式
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
;(2)上图装置还可以用于完成某些固体物质受热分解的实验.请回答:
①Na2CO3和NaHCO3这两种物质中有一种可以用上图装置进行受热分解的实验.该物质受热分解的化学反应方程式为:
2NaHCO3
Na2CO3+H2O+CO2↑
| ||
2NaHCO3
Na2CO3+H2O+CO2↑
;
| ||
②为了验证①中该物质受热分解产生的所有气体产物,在虚线处应连接(表述时请指明使用仪器,仪器中盛装的试剂和仪器的连接顺序)
先连接装有白色无水硫酸铜固体的干燥管,再连接装有澄清石灰水的烧杯
先连接装有白色无水硫酸铜固体的干燥管,再连接装有澄清石灰水的烧杯
;③请提出一点有关实验过程中安全问题的建议:
反应后先撤导气管,再撤酒精灯
反应后先撤导气管,再撤酒精灯
;④如果将12.6g的该物质加热分解,加热一段时间后,测得剩余固体质量为9.5g,则已经分解的该物质的质量为
8.4
8.4
g.分析:(1)①氨气密度小于空气的密度;氨气能够使湿润的红色石蕊试纸变蓝;
②氨气极易溶于水;
③实验室用氯化铵和氢氧化钙加热反应制取氨气;
(2)①NaHCO3 加热容易分解;
②分解气体产物有二氧化碳和水,先检验水,再检验二氧化碳,不能颠倒;
③反应完毕,不能先撤酒精灯;
④写出反应方程式,设分解的碳酸氢钠质量为xg,利用质量差求算.
②氨气极易溶于水;
③实验室用氯化铵和氢氧化钙加热反应制取氨气;
(2)①NaHCO3 加热容易分解;
②分解气体产物有二氧化碳和水,先检验水,再检验二氧化碳,不能颠倒;
③反应完毕,不能先撤酒精灯;
④写出反应方程式,设分解的碳酸氢钠质量为xg,利用质量差求算.
解答:解:(1)①由于氨气密度小于空气的密度,收集时采用向下排空气法,检验氨气采用的是 湿润的红色石蕊试纸,故答案为:瓶口向下排空气法;用湿润的红色石蕊试纸靠近瓶口,试纸变蓝,说明已收集满;
②氨气极易溶于水,可以完成喷泉实验,故答案为:极易溶于水;
③氢氧化钙和氯化铵可以制取氨气,反应的方程式为2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O;
(2)①碳酸钠不易分解,碳酸氢钠加热会分解,反应的方程式为:2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:2NaHCO3
Na2CO3+H2O+CO2↑;
②分解方程式为,2NaHCO3
Na2CO3+2H2O+CO2↑,产物中有H2O和CO2气体,必须先检验水,用白色的无水硫酸铜检验;再检验二氧化碳,用澄清石灰水,故答案为:先连接装有白色无水硫酸铜固体的干燥管,再连接装有澄清石灰水的烧杯;
③反应后不能先撤酒精灯,防止水倒流进入试管,发生危险,故答案为:反应后先撤导气管,再撤酒精灯;
④设分解的碳酸钠为xg,反应方程式为:2NaHCO3
Na2CO3+H2O+CO2↑,△m
168g 106g 62g
xg (12.6-9.5)g
列式为:168×(12.6-9.5)=62x,解得x=8.4(g),
故答案为:8.4.
②氨气极易溶于水,可以完成喷泉实验,故答案为:极易溶于水;
③氢氧化钙和氯化铵可以制取氨气,反应的方程式为2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O;
(2)①碳酸钠不易分解,碳酸氢钠加热会分解,反应的方程式为:2NaHCO3
| ||
| ||
②分解方程式为,2NaHCO3
| ||
③反应后不能先撤酒精灯,防止水倒流进入试管,发生危险,故答案为:反应后先撤导气管,再撤酒精灯;
④设分解的碳酸钠为xg,反应方程式为:2NaHCO3
| ||
168g 106g 62g
xg (12.6-9.5)g
列式为:168×(12.6-9.5)=62x,解得x=8.4(g),
故答案为:8.4.
点评:本题考查氨气的制取和性质,是一道较综合的实验题,内容较丰富,难度适中.

练习册系列答案
相关题目
 看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)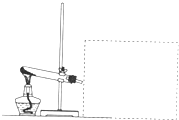 看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)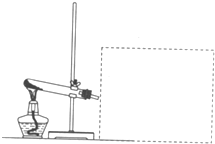 看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)