题目内容
(2007?资阳二模)已知反应A2(g)+2B2(g)?2AB2(g)(正反应为放热反应),下列说法正确的是( )
分析:升高温度,正逆反应速率都增大,因正反应为放热反应,则平衡向逆反应方向移动,逆反应速率大于正反应速率,反应物气体的计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,反之向左移动,以此解答该题.
解答:解:升高温度,正逆反应速率都增大,可缩短得到平衡所用时间,则A错误、B正确;
因正反应为放热反应,则平衡向逆反应方向移动,反应物气体的计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,则C、D错误.
故选B.
因正反应为放热反应,则平衡向逆反应方向移动,反应物气体的计量数之和大于生成物气体的化学计量数之和,则增大压强平衡向正反应方向移动,则C、D错误.
故选B.
点评:本题考查化学反应速率,为高考高频考点,侧重于反应速率的影响因素的考查,能较好的培养学生良好的科学素养,难度不大,答题时注意把握方程式的特征,如气体的体积关系以及反应热等问题,为解答该题的关键.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
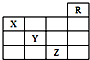 (2007?资阳二模)如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
(2007?资阳二模)如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )