题目内容
在C2H6、C3H6、C4H6三种气体中,任意取两种气体混合后,充分燃烧,消耗氧气的体积为混合气体原体积的5倍(同温同压下)。求混合气体中符合此要求的可能组合及两种气体的物质的量之比(要有简单计算推断过程)
解:三种烃分子中氢原子数均为6,可设混合烃的平均分子式为CnH6则有
2CnH6+(2n+3)O2![]() 2nCO2+6H2O
2nCO2+6H2O
2 2n+3
1 5
解得n=3.5,则混合烃的平均分子式为C3.5H6.由平均分子式看出,混合气体中肯定有C4H6,混合气体的组合为:C4H6和C2H6,C4H6和C3H6 其物质的量之比
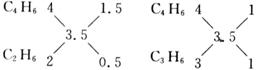 C4H6和C2H6物质的量之比为3:1;C4H6和C3H6其物的量之比为1:1。
C4H6和C2H6物质的量之比为3:1;C4H6和C3H6其物的量之比为1:1。

练习册系列答案
相关题目
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
|
仔细分析下列表格中烃的排布规律,判断排列在第12位的烃的同分异构体的数目是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
| C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4Hl0 | … |
| A、3 | B、4 | C、5 | D、6 |
仔细分析下列表格中烃的排列规律,判断排列在第16位烃的分子式是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
| C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | … |
| A、C6H12 |
| B、C6H14 |
| C、C7H12 |
| D、C7H14 |