题目内容
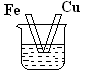
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:

(1) 锌片上发生的电极反应: ;
铜片上发生的电极反应: ;
(2)若该电池中两电极的总质量为60g,工作一段时间后,
取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况
氢气的体积为多少L?

(1) 锌片上发生的电极反应: ;
铜片上发生的电极反应: ;
(2)若该电池中两电极的总质量为60g,工作一段时间后,
取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况
氢气的体积为多少L?
(1)Zn-2e-=Zn2+ 2H++2e-=H2↑ (每空2分) (2) 4.48 L(4分)
(1)锌比铜活泼,所以在该原电池中锌作负极,失去电子被氧化。铜作正极,溶液中的氢离子达到电子,被还原,生成氢气。
(2)反应前后电极质量减少了60g-47g=13g,所以溶解的锌的质量就是13g,物质的量为 ,反应中转移电子0.2mol×2=0.4mol。根据得失电子守恒可知生成氢气的物质的量是0.2mol,所以其体积是0.2mol×22.4L/mol=4.48L。
,反应中转移电子0.2mol×2=0.4mol。根据得失电子守恒可知生成氢气的物质的量是0.2mol,所以其体积是0.2mol×22.4L/mol=4.48L。
(2)反应前后电极质量减少了60g-47g=13g,所以溶解的锌的质量就是13g,物质的量为
 ,反应中转移电子0.2mol×2=0.4mol。根据得失电子守恒可知生成氢气的物质的量是0.2mol,所以其体积是0.2mol×22.4L/mol=4.48L。
,反应中转移电子0.2mol×2=0.4mol。根据得失电子守恒可知生成氢气的物质的量是0.2mol,所以其体积是0.2mol×22.4L/mol=4.48L。
练习册系列答案
相关题目