题目内容
(8分)A是由C、H或C、H、O元素组成的有机物,取0.01 mol A在1.456 L(标准状况)氧气中燃烧,燃烧后的产物通过足量浓硫酸,浓硫酸增重0.54 g,再在通过浓硫酸后的气体中点燃Mg条(足量),生成总质量为5.16 g的黑白两种物质,且黑色生成物与白色生成物的物质的量比为1∶4。求A的分子式。
C3H6O2
因黑色生成物(C)与白色生成物(MgO)的物质的量之比为1∶4,故氧气过量。通过浓硫酸后的气体为CO2和O2的混合物。设Mg与O2、CO2反应分别生成MgO的物质的量为x、y:
2Mg+O2="===2MgO " 2Mg+CO2====2MgO+C
0.5x x y 0.5y

解得:x="y=0.06" mol,过量的n(CO2)="0.03" mol,生成的n(CO2)="0.03" mol,生成的n(H2O)="0.54" g/18 g·mol-1="0.03" mol。0.01 mol A的质量m(A)=[0.03×44+0.54-(1.456÷22.4-0.03)×32] g="0.74" g,M(A)= ="74" g·mol-1
="74" g·mol-1
设A的分子式为C3H6Oz,有3×12+6×1+16z=74,z=2,A的分子式为C3H6O2。
2Mg+O2="===2MgO " 2Mg+CO2====2MgO+C
0.5x x y 0.5y

解得:x="y=0.06" mol,过量的n(CO2)="0.03" mol,生成的n(CO2)="0.03" mol,生成的n(H2O)="0.54" g/18 g·mol-1="0.03" mol。0.01 mol A的质量m(A)=[0.03×44+0.54-(1.456÷22.4-0.03)×32] g="0.74" g,M(A)=
 ="74" g·mol-1
="74" g·mol-1设A的分子式为C3H6Oz,有3×12+6×1+16z=74,z=2,A的分子式为C3H6O2。

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
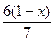
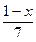
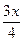
 C6H5OH+NaHCO3
C6H5OH+NaHCO3
 KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。
KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。