题目内容
17.25℃,对于1L1mol•L-1CuSO4溶液和1L1mol•L-1FeCl3溶液,下列说法正确的是( )| A. | 前者溶液为黄色,后者为蓝色 | |
| B. | 加入1L1mol•L-1Na2CO3溶液后都能大量共存 | |
| C. | 加入28g还原铁粉,都发生氧化还原反应 | |
| D. | 都可以催化H2O2的分解,且催化效果相同 |
分析 A.含铜离子的溶液为蓝色,含铁离子的溶液为黄色;
B.铜离子、铁离子均与碳酸根离子反应;
C.Fe与硫酸铜反应生成Cu,Fe与氯化铁反应生成氯化亚铁;
D.FeCl3溶液对H2O2的分解催化作用好.
解答 解:A.含铜离子的溶液为蓝色,含铁离子的溶液为黄色,则前者为蓝色,后者为黄色,故A错误;
B.铜离子、铁离子均与碳酸根离子反应,则加入Na2CO3溶液后都不能大量共存,故B错误;
C.Fe与硫酸铜反应生成Cu,Fe与氯化铁反应生成氯化亚铁,单质Fe中Fe元素的化合价均升高,均发生氧化还原反应,故C正确;
D.催化剂具有专一性,FeCl3溶液对H2O2的分解催化作用好,故D错误;
故选C.
点评 本题考查金属化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
7.相对分子质量为86的烷烃,有几种同分异构体( )
| A. | 6 | B. | 5 | C. | 4 | D. | 3 |
8.联氨(N2H4)和N2O4可作为火箭推进剂.已知:
①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2O4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=-1048.9kJ/mol-1
下列叙述不正确的是( )
①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2O4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=-1048.9kJ/mol-1
下列叙述不正确的是( )
| A. | △H3不是H2(g)的燃烧热 | |
| B. | △H4=2△H 3-2△H2-△H1 | |
| C. | 联氨和N2O4反应放热多、产生大量气体,因此可作为火箭推进剂 | |
| D. | 若联氨为气态,△H4大于-1048.9kJ?mol-1 |
5.化学与生活和环境密切相关,下列有关说法中错误的是( )
| A. | 食品包装中常放有硅胶,能起到干燥的作用 | |
| B. | 用工业酒精兑制饮用酒出售来提高利润 | |
| C. | 明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒作用 | |
| D. | 集中处理废旧电池,以防止污染 |
12.X、Y、W、Z均为短周期元素,在周期表中位置如图所示,其中X原子的最外层电子数比次外层的电子数少5个.下列说法不正确的是( )
| W | Z | |
| X | Y |
| A. | 原子半径:X>Y>W>Z | |
| B. | W的氧化物都能与碱反应生成盐和水 | |
| C. | X的单质与Fe2O3高温下可发生反应 | |
| D. | Y的单质可用于制作半导体材料 |
2.下列说法正确的是( )
| A. | 乙烯和聚乙烯都可以与溴水发生加成反应 | |
| B. | 在浓硫酸作催化剂条件下,加热乙醇不一定得到乙烯 | |
| C. | 苯酚在空气中显淡红色,并未变质 | |
| D. | 甲苯最多有15个原子在同一个平面 |
9.下列关于苯的叙述正确的是( )
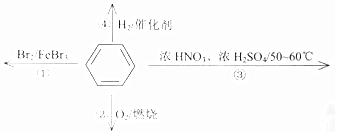

| A. | 反应①为取代反应,有机产物与水混合浮在上层 | |
| B. | 反应②为氧化反应,反应现象是火焰明亮并有大量黑烟 | |
| C. | 反应③为取代反应,控制反应温度在50~60℃的方法是用酒精灯直接加热 | |
| D. | 反应④中1mol苯最多与3molH2发生加成反应,原因是苯分子含有三个碳碳双键 |
6.下列有机物的说法,正确的是( )
| A. | 等物质的量的甲烷与氯气反应后体积保持不变 | |
| B. | 石蜡油、苯、环己烷都不能使溴的四氯化碳溶液褪色 | |
| C. | 分子式为C5H12的有机物有三种,它们互为同系物 | |
| D. | C4H8Cl2有8种同分异构体(不考虑立体异构) |