��Ŀ����
����Ŀ����ѧϰ��Ԫ��������֮��ij��ѧʵ��С�����������ʵ�飬��֤̼Ԫ�صķǽ����Աȹ�Ԫ�صķǽ�����ǿ����ش��������⣺
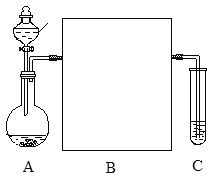
(1)װ��A�ķ�Һ©����ʢװ���Լ���_____����ƿ�м����״������_____��
(2)װ��C��ʢ�ŵ��Լ���_____(ѡ����ĸ)
A��Na2CO3��Һ B��Na2SiO3��Һ C��NaOH��Һ
(3)����ʵ�߿��ڵ�ʵ��װ��ͼ����ע�������Լ�����װ�õ�������_____��
(4)C��ʵ������Ϊ_____����ѧ��Ӧ����ʽ��_____����û��Bװ�ã���ȻC�г��ֵ�������ͬ����Ҳ���ܵó���ȷ���ۣ�ԭ����_____��
(5)��̼���������ڱ��е�λ�ýǶȣ���Ҫ����̼Ԫ�صķǽ����Աȹ�Ԫ�صķǽ�����ǿ��ԭ����_____��
(6)������Щ��ʵ�ܹ�˵��̼Ԫ�صķǽ����Աȹ�Ԫ�صķǽ�����ǿ(�Ծ�һ��)_____��
���𰸡�ϡ���� ̼��� B 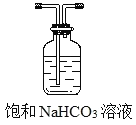 ��ȥCO2 �е�HCl ���� ���ֻ��ǻ��ɫ��״���� CO2 + H2O + Na2SiO3 = Na2CO3 + H2SiO3�� �������Աȹ���ǿ��HCl ��Na2SiO3 ��Һ��ӦҲ����� H2SiO3 ���� ���߾�Ϊ�ڢ�A ��Ԫ�أ�̼Ԫ�������ڱ���λ�ڹ�Ԫ���Ϸ���ͬ��Ԫ�ش��ϵ��·ǽ����Լ���������������ˮ��������Լ��� CH4 ���ȶ���ǿ��SiH4
��ȥCO2 �е�HCl ���� ���ֻ��ǻ��ɫ��״���� CO2 + H2O + Na2SiO3 = Na2CO3 + H2SiO3�� �������Աȹ���ǿ��HCl ��Na2SiO3 ��Һ��ӦҲ����� H2SiO3 ���� ���߾�Ϊ�ڢ�A ��Ԫ�أ�̼Ԫ�������ڱ���λ�ڹ�Ԫ���Ϸ���ͬ��Ԫ�ش��ϵ��·ǽ����Լ���������������ˮ��������Լ��� CH4 ���ȶ���ǿ��SiH4
��������
�ǽ�����ǿ����Ϊ��ۺ����������ǿ�ȶ�棬�Ƚ�����ǿ�������ø��ֽⷴӦ�н�ǿ�����ɽ�����Ĺ��ɡ�ʵ������б����ֹ���ʵĸ��ţ��Ա�֤ʵ����۵Ŀɿ��ԡ�
��֤�ǽ�����C>Si��ͨ����֤����H2CO3>H2SiO3�������Ʊ�CO2�����ӣ���ͨ��Na2SiO3��Һ�С�
(1)װ��A��CO2����װ�ã� ��ƿ�еĿ�״������ʯ��ʯ�����ʯ����Һ©����ʢװϡ���
(2)װ��C ��ʢ�ŵ��Լ���Na2SiO3��Һ��
(3)�����������Ƶõ�CO2�л��лӷ�����HCl���ʣ�Ϊ��ֹ����C�е�Na2SiO3��Һ��Ӧ���ʽ�������ͨ��ʢ�б���NaHCO3��Һ��ϴ��ƿ��
(4)C�����ɵĹ������ˮ������Ϊ���ֻ��ǻ��ɫ��״��������ѧ����ʽ��CO2 + H2O + Na2SiO3 = Na2CO3 + H2SiO3������û��B װ�ã�����HCl ��Na2SiO3 ��Һ��ӦҲ����� H2SiO3 ������
(5)�����ڱ���̼����ͬ�ڵ�IVA�壬ͬ����Ԫ�ش��ϵ��·ǽ����Լ�������̼Ԫ�صķǽ����Աȹ�Ԫ�صķǽ�����ǿ��
(6)CH4 ���ȶ���ǿ��SiH4��SiC��̼Ԫ�سʣ�4�۵ȵȣ�����˵��̼Ԫ�صķǽ����Աȹ�Ԫ�صķǽ�����ǿ��


