��Ŀ����
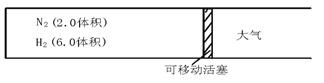
��һ���¶��£���2 mol SO2��1 mol O2ͨ��һ��һ���ݻ����ܱ�������������·�Ӧ��2SO2+O2![]() 2SO3�����˷�Ӧ���е�һ���̶�ʱ����Ӧ�����ʹ��ڻ�ѧƽ��״̬�����ڸ������У�ά���¶Ȳ��䣬��a��b��c���ֱ������ʼ�����SO2��O2��SO3�����ʵ�����Ħ�������a��b��cȡ��ͬ����ֵ�����DZ�������һ�������ϵ�����ܱ�֤�ﵽƽ��ʱ����Ӧ������������������������Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף�
2SO3�����˷�Ӧ���е�һ���̶�ʱ����Ӧ�����ʹ��ڻ�ѧƽ��״̬�����ڸ������У�ά���¶Ȳ��䣬��a��b��c���ֱ������ʼ�����SO2��O2��SO3�����ʵ�����Ħ�������a��b��cȡ��ͬ����ֵ�����DZ�������һ�������ϵ�����ܱ�֤�ﵽƽ��ʱ����Ӧ������������������������Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף�
��1����a=0��b=0��c=_____________��
��2����a=0.5����b=_____________��c=____________��
��3��a��b��cȡֵ���������һ�������ǣ�����������ʽ��ʾ������һ��ֻ��a��c����һ��ֻ��b��c��:_____________��______________��
��1��2 ��2��0.25 1.5 ��3��a+c=2 2b+c=2
����:
��һ�������µĿ��淴Ӧ���Ӧ�����Ǵ�����ʼ���Ǵ�����ʼ�����ɴ�ͬһƽ��״̬������һ���¶��µĿ��淴Ӧ��2SO2+O2![]() 2SO3����ʼ̬��2 mol SO2��1 mol O2�����ʼ̬Ϊ2 mol SO3�����ƽ��״̬��ȫ��ͬ������a=0��b=0��c=2������ʼSO2Ϊ0.5 mol ������ʼO2ӦΪSO2������һ�뼴0.25 mol����ʼSO3Ϊ1.5 molʱ���ſ��ܴﵽ��������ȫ��ͬ��ƽ��״̬����������ֻ֪�н���ʼ�ﶼת��Ϊ��Ӧ��SO2��O2ʱ���õ��൱��2 mol SO2��1 mol O2���Ϳɴﵽ�����������ȫ��ͬ��ƽ��״̬����2SO2+O2=2SO3���Ƴ���a+c=2��b+
2SO3����ʼ̬��2 mol SO2��1 mol O2�����ʼ̬Ϊ2 mol SO3�����ƽ��״̬��ȫ��ͬ������a=0��b=0��c=2������ʼSO2Ϊ0.5 mol ������ʼO2ӦΪSO2������һ�뼴0.25 mol����ʼSO3Ϊ1.5 molʱ���ſ��ܴﵽ��������ȫ��ͬ��ƽ��״̬����������ֻ֪�н���ʼ�ﶼת��Ϊ��Ӧ��SO2��O2ʱ���õ��൱��2 mol SO2��1 mol O2���Ϳɴﵽ�����������ȫ��ͬ��ƽ��״̬����2SO2+O2=2SO3���Ƴ���a+c=2��b+![]() =1��2b+c=2��
=1��2b+c=2��

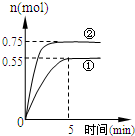 ̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ��
̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ��