题目内容
一定温度下的密闭容器中存在如下反应:
CO(g)+H2O(g)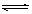 CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡_______,若未达到平衡,向哪个方向进行______。
(2)达到平衡时,CO的转化率____________________。
(3)当CO的起始浓度仍为2 mol·L-1,H2O(g)的起始浓度为6 mol·L-1,求平衡时CO的转化率_______。
CO(g)+H2O(g)
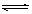 CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:(1)当CO转化率为25%时,该反应是否达到平衡_______,若未达到平衡,向哪个方向进行______。
(2)达到平衡时,CO的转化率____________________。
(3)当CO的起始浓度仍为2 mol·L-1,H2O(g)的起始浓度为6 mol·L-1,求平衡时CO的转化率_______。
(1)反应未达平衡 Q=1∕9<K=1,平衡向正反应方向进行。(2)50℅ (3) 75℅。
试题分析:(1)当CO转化率为25%时则{C(CO2)C(H2)}∕{C(CO)C(H2O)}=(0.5×0.5)∕(1.5×1.5)=1∕9<1.所以反应未达到平衡。反应向正反应方向进行。当反应达到平衡时,假设消耗的CO浓度为x,根据反应方程式中各物质的关系可得X2∕(2-X)2=1.解得X="1," CO转化率为(1∕2)×100℅=50℅。(3)假设在这种条件下,达到平衡时CO消耗了a mol·L-1,则平衡时各物质的浓度为C(CO)=(2- a)mol·L-1 C(H2O)=(6-a)mol·L-1C(CO2)=amol·L-1C(H2)=amol·L-1. a2∕{(2- a)×(6-a)}=1解得a=1.5.所以CO的转化率为: (1.5∕2) ×100℅=75℅。

练习册系列答案
相关题目
 I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是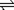 xC(g) ΔH 有:
xC(g) ΔH 有: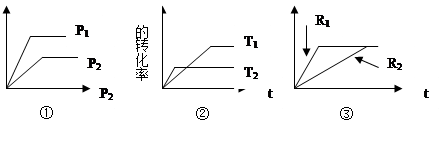
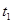 s后达平衡。如图:
s后达平衡。如图:
 H2+I2(g)在密闭容器中装入1molHI气体在一定条件下使它分解,已知有35%发生分解,则容器内混合气体的总物质的量是
H2+I2(g)在密闭容器中装入1molHI气体在一定条件下使它分解,已知有35%发生分解,则容器内混合气体的总物质的量是 Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入
Cr2O72-(橙红色)+ H2O中,溶液介于黄和橙红色之间,今欲增加溶液的橙红色,则要在溶液中加入 C(g)+D(g)已达平衡状态的是( )
C(g)+D(g)已达平衡状态的是( )